167 4T-MMDA-2
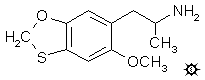
6-(2-AMINOPROPYL)-5-METHOXY-1,3-BENZOXATHIOL; 2-METHOXY-4,5-METHYLENETHIOOXYAMPHETAMINE 6-(2-氨基丙基)-5-甲氧基-1,3-苯并氧杂硫杂茂;2-甲氧基-4,5-亚甲硫氧基苯丙胺
 |
|---|
合成: 向搅拌良好的 120 g 硫脲溶于 800 mL 2N 盐酸的溶液中,在 15 分钟内加入 100 g 苯醌溶于 500 mL 乙酸的溶液。在室温下继续搅拌 0.5 小时,然后在蒸汽浴上加热反应混合物 1 小时。在冰水中冷却,析出大量晶体。过滤去除并风干,得到 90.1 g 5-羟基-1,3-苯并氧杂硫杂茂-2-酮(2-巯基对苯二酚环状碳酸酯),熔点为 170.5-172.5 °C。
向 100 g 细粉状无水碳酸钾悬浮于含有 50 g 碘甲烷的 400 mL 丙酮中,加入 41 g 5-羟基-1,3-苯并氧杂硫杂茂-2-酮,混合物在室温下搅拌过夜。过滤去除固体,真空去除溶剂。蒸馏残留物,得到一个在 110 °C 烘箱温度和 0.1 mm/Hg 下升华出来的固体馏分。这是一种淡黄色固体,重 27.4 g,熔点为 66-72 °C。用甲醇重结晶得到 5-甲氧基-1,3-苯并氧杂硫杂茂-2-酮,为白色固体,熔点 75.5-76.5 °C。
向 30 g 85% 氢氧化钾溶于 75 mL 温水的溶液中,加入等体积的温甲醇,随后加入 16 g 5-甲氧基-1,3-苯并氧杂硫杂茂-2-酮,混合物回流 2 小时。冷却至室温后,混合物用盐酸酸化并用 2x100 mL 二氯甲烷提取。合并提取液去除溶剂后,得到黄色油状物,静置结晶。产物 2-巯基-4-甲氧基苯酚重 14 g,熔点 56-57 °C。
将 10 g 2-巯基-4-甲氧基苯酚溶于 100 mL 甲乙酮的溶液在 1 小时内加入到剧烈搅拌的 25 g 细粉状无水碳酸钾悬浮于含有 14 g 二溴甲烷的 200 mL 甲乙酮中。保持回流 48 小时。冷却后,过滤去除固体,滤饼用额外的 50 mL 甲乙酮洗涤。合并洗涤液和滤液,在真空下去除溶剂,蒸馏产物得到 3.3 g 5-甲氧基-1,3-苯并氧杂硫杂茂,为变黄的油状物,沸点 110-120 °C (1.7 mm/Hg)。釜中有相当多的残留物被丢弃。核磁共振谱极好,亚甲基质子在 5.6 ppm 处显示为双氢单峰。
向 3.2 g 三氯氧磷和 2.8 g N-甲基甲酰苯胺的混合物(已在蒸汽浴上短暂加热至形成深紫红色)中加入 2.3 g 5-甲氧基-1,3-苯并氧杂硫杂茂,并在蒸汽浴上继续加热 5 分钟。将反应混合物倒入 100 mL 水中,搅拌几分钟后,不溶物变为松散的固体。过滤收集,水洗,尽可能抽干后,用 30 mL 沸腾的甲醇重结晶。得到 1.9 g 6-甲酰基-5-甲氧基-1,3-苯并氧杂硫杂茂,为褐色针状晶体,熔点 119-120 °C。
将 1.5 g 6-甲酰基-5-甲氧基-1,3-苯并氧杂硫杂茂溶于 50 mL 硝基乙烷的溶液用 0.3 g 无水乙酸铵处理,并在蒸汽浴上加热 5 小时。真空去除溶剂得到结晶残留物。用 110 mL 沸腾的乙醇重结晶,过滤并风干后,得到 1.3 g 5-甲氧基-6-(2-硝基-1-丙烯基)-1,3-苯并氧杂硫杂茂,为旧金山巨人队橙色的晶体。
在 0 °C 和氦气下,向 1.3 g 氢化锂铝溶于 10 mL 四氢呋喃的溶液中加入 0.8 mL 100% 硫酸,制备氢化铝(AH)溶液。逐滴加入 1.1 g 5-甲氧基-6-(2-硝基-1-丙烯基)-1,3-苯并氧杂硫杂茂溶于 25 mL 四氢呋喃的溶液,继续搅拌 1 小时。短暂回流后,使反应混合物恢复至室温,并加入异丙醇破坏过量的氢化物。加入 5% 氢氧化钠将盐转化为可过滤的块状物,过滤并用异丙醇洗涤后,合并滤液和洗涤液并在真空下去除溶剂。残留物溶解于稀硫酸中,用 3x75 mL 二氯甲烷洗涤,然后用 25% 氢氧化钠碱化,产物用 2x75 mL 二氯甲烷提取。合并提取液,真空去除溶剂。蒸馏残留物得到一个沸点为 140-155 °C (0.3 mm/Hg) 的馏分,重 0.7 g。将其溶解于 4 mL 异丙醇中,用 14 滴浓盐酸中和,加热使其完全溶解,然后用 10 mL 无水乙醚稀释。去除形成的白色晶体,乙醚洗涤并风干,得到 0.6 g 6-(2-氨基丙基)-5-甲氧基-1,3-苯并氧杂硫杂茂盐酸盐 (4T-MMDA-2)。
给药剂量: 大于 25 mg。
药效时长: 未知。
定性评论: (摄入 25 mg)服药三小时后,我觉得可能有一点兴奋感。也许还有一丝颤抖和咬牙。这可能是一个阈值剂量。
延伸和评论: 没有逻辑方法可以猜测这种物质的活性水平在哪里。在比较 4-氧代与 4-硫代和 4-烷基(例如 TMA-2,PARA-DOT 和 DOM)时,具有硫原子的类似物在效力上介于氧原子和碳原子之间。那么,也许 4T-MMDA-2 应该比 MMDA-2 稍微强效一些。这就是试验所达到的程度,而缺乏效果因此宣告该推理无效。还有什么可以用作线索?整个苯并呋喃项目,具有相同的环状性质,也没有活性。它们在 4T-MMDA-2 的硫所在的位置有一个碳,所以,按照这种计算,这种化合物的活性应该更低。也许这就是要遵循的公式。底线是不可避免的。这些推断都比不上唯一能给出可信结果的实验,即新化合物在人体内的实际试验。
这里使用的杂环碳酸酯的位置异构体也是已知的。如果不使用苯醌作为起始原料并用硫脲作为硫源(产生 1,4-氧取向),而是从间苯二酚开始,与硫氰酸铵作为硫源反应(在硫酸铜存在下),则得到具有 1,3-氧取向的位置异构体。这种材料(也称为 thioxolone 或 tioxolone,或 6-羟基-1,3-苯并氧杂硫杂茂-2-酮,市面有售)应该遵循这里展示的 5-羟基类似物的相同化学反应,并最终得到 5T-MMDA-2(5-(2-氨基丙基)-6-甲氧基-1,3-苯并氧杂硫杂茂或 2-甲氧基-5,4-亚甲硫氧基苯丙胺)。根据比较 5-TOM 与 DOM 的发现,我猜测这将是一种效力相对较低的化合物。至少它应该很容易制造!