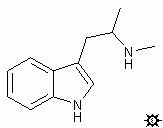
8.a,N-DMT
色胺,a,N-二甲基;吲哚,3-[2-(甲氨基)丙基];a,N-二甲基色胺;3-[2-(甲氨基)丙基]吲哚;ALPHA-N
 |
|---|
合成:(从吲哚丙酮出发)向 1.55 克乙酸钠溶于 5 毫升乙酸酐的溶液中加入 2.0 克 3-吲哚乙酸,混合物在 135-140 °C 下加热 18 小时。在旋转蒸发仪上减压除去所有挥发物,产生淡黄色残留物,即 1-乙酰基吲哚-3-丙酮。将其溶于甲醇中,加入 0.93 克甲醇钠,溶液回流数小时。减压除去溶剂后,将残留物悬浮在水中并用几份乙醚提取。合并提取液,减压除去溶剂得到 0.41 克(21%)吲哚-3-丙酮,为白色固体,熔点 115-117 °C。质谱(m/z):吲哚甲基+ 130 (100%);分子离子峰 173 (16%)。红外(cm-1):691, 753, 761, 780, 1017, 1110, 1172,以及 1710 处的宽 C=O 峰。
向 1 克碎铝箔中加入 20 毫克氯化汞溶于 15 毫升水的溶液。15 分钟后,滤掉汞溶液,用新鲜水洗净汞齐化铝,并尽可能摇干。然后依次加入 1.5 克甲基胺盐酸盐溶于 2 毫升水的溶液、3 毫升 25% 氢氧化钠、5 毫升异丙醇,最后加入 1 克吲哚-3-丙酮溶于 20 毫升异丙醇的溶液。搅拌 1 小时,然后在蒸汽浴上短暂加热。冷却后,过滤反应混合物,固体用甲醇洗涤,合并洗液和滤液,减压除去溶剂。残留物溶于 200 毫升水中,用盐酸酸化,用二氯甲烷洗涤,用氢氧化钠水溶液处理至 pH 大于 9(变浑浊),并用 2x50 毫升二氯甲烷提取。从合并的提取液中除去溶剂得到浅褐色油状物,在 0.4 mm/Hg 下、125-135 °C 下蒸馏,得到 0.74 克粘稠油状物。将其溶于 5 毫升异丙醇中,用浓盐酸中和,并用无水乙醚稀释至浑浊。静置后,滤出固体,用乙醚洗涤并空气干燥,得到 0.87 克 a,N-二甲基色胺盐酸盐(a,N-DMT),为白色晶体。质谱(m/z):C3H8N+ 58 (100%);吲哚甲基+ 131-130 (19, 14%);分子离子峰 188,仅略高于噪声水平。
或者,吲哚-3-丙酮可以在甲胺存在下催化还原。将 3.3 克吲哚-3-丙酮溶于 100 毫升乙醇中,在过量甲胺存在下用钯碳催化剂氢化。2 小时后,通过过滤除去催化剂,滤液减压除去溶剂,残留物溶于水并酸化。用乙醚洗涤后,水相碱化,形成的固体通过过滤除去,并从己烷和四氢呋喃的混合物中重结晶。产物 a,N-二甲基色胺(a,N-DMT)为褐色固体,重 2.2 克,熔点 93-94 °C。苦味酸盐从乙醇中结晶为砖红色,熔点 207-208 °C。
(从 a-MT 出发)将 4.4 克 alpha-甲基色胺(a-MT)溶于含有 3.1 克乙酸和 2.4 克甲酸的 5.5 克乙酸酐溶液中,在室温下搅拌 18 小时。在低于 40 °C 的温度下减压除去所有挥发物,留下糖浆状残留物。向其中加入 100 毫升水,用几份乙醚提取,合并乙醚相并减压除去溶剂。残留 4.9 克(95%)的 a-甲基-N-甲酰基色胺,直接用于下一步。将其溶于 30 毫升无水四氢呋喃中,在氮气保护下,将该溶液加入到 3.7 克氢化铝锂(LAH)悬浮于 30 毫升四氢呋喃的微沸悬浮液中,反应 16 小时。冷却后,通过小心加入湿四氢呋喃破坏过量的氢化物,随后加入足够的氢氧化钠水溶液以产生易于通过过滤除去的固体。过滤后,滤液减压除去溶剂,残留物(4.3 克)从苯/石油醚中结晶,得到 2.5 克(56%)的 a,N-二甲基色胺(a,N-DMT),为固体,熔点 90-91 °C。N-乙基同系物由 a-甲基-N-乙酰基色胺以类似方法制得,熔点 187-189 °C。
给药剂量:50 - 100 毫克
药效时长:6 - 8 小时
定性评论:(50 毫克,口服)“有些事情正在发生,在开始两小时后相当强烈,但这里似乎没有任何特别的致幻效果。我清醒且警觉,也许有点像戴了度数不对的眼镜一样眼花缭乱。也许还有一点头重脚轻。过了几个小时,这些身体不适才消失。”
(75 毫克,口服)“强迫性打喷嚏,非常不舒服。想吐。试着吃点法式咸派,但吃不下——完全没有食欲。脉搏似乎正常,但感觉就像是在使用没有任何兴奋优点的苯丙胺。大约三四个小时后,我正在失去那种嗡嗡的感觉,再过三四个小时就基本正常了。仍然有些咬牙。睡眠还可以。我不确定更高剂量是否值得。甚至不确定是否值得重复。为什么?”
延伸和评论:a-MT(alpha-甲基色胺)与该化合物 a,N-DMT(alpha,N-二甲基色胺)之间的关系,与苯乙胺对应物中苯丙胺(alpha-甲基苯乙胺)和甲基苯丙胺(alpha,N-二甲基苯乙胺)之间的关系完全类似。伯胺和仲胺化合物都保留了活性。在苯丙胺阵营中,这两种化合物都是强效兴奋剂,表现出完整的拟交感神经特性,包括心血管兴奋、食欲丧失和失眠。在这里,色胺对应物彼此相似,但并不明确它们是兴奋剂。在动物研究中,它们被拿来互相比较,并与苯丙胺比较。除了起效速度外,两种色胺在活动笼中都引起了类似苯丙胺的行为,但需要的剂量约为苯丙胺的 10 倍。在人类身上有一些这方面的迹象,如食欲丧失、嗡嗡的头晕感,以及没有任何通常的致幻作用迹象。
我在 a-MT 的评论中提到了一个吸引人的假设,它也适用于这里。a-MT 和 a,N-DMT 这两种物质都是有效的单胺氧化酶抑制剂。这两种物质都表现出一些已被描述为 beta-卡巴啉家族单胺氧化酶抑制剂的综合征。设计并进行一项研究,探讨其中任何一种在促进死藤水物质口服活性方面的作用将很有趣,这些物质单独服用时会被脱氨基从而失活。这整个论点可以而且应该包含甲氧基化对应物 a,N,O-TMS。我不知道有任何关于其脱氨酶促有效性的研究,但它也符合这里显示的恶心、不适、非致幻模式。由于 5-甲氧基引起的预期效力增加是正常的,使其成为比这两个更有效的化合物。让我们也把它纳入研究。
在所有这些案例中,向氮原子添加一个额外的甲基会产生叔胺。在苯乙胺类比中,会得到 N,N-二甲基苯丙胺。几年前,这种化合物出现在几个秘密的甲基苯丙胺实验室中,原因是厨师用 N-甲基麻黄碱代替了常用的前体麻黄碱。虽然对 N,N-二甲基苯丙胺的动物研究表明它几乎没有任何兴奋特性,但当局认为,既然它出现在非法背景中(可能被作为街头药物贩卖),它就具有真正的滥用潜力。而且由于它没有公认的医疗用途,它显而易见的归宿就是《受控物质法案》的附表 I。它确实被放在了那里。
将这种结构修饰应用于色胺领域,得到了 alpha,N,N-三甲基色胺(a,N,N-TMT)。苯乙胺中的叔胺 N,N-二甲基苯丙胺表现出兴奋性质的丧失。在这里,添加那个额外的甲基得到一个具有 DMT 骨架的叔胺。据报道,该碱可以通过两种不同的路线制得,均从吲哚开始。与环氧丙烷反应得到 3-吲哚基-2-丙醇,先用三溴化磷处理,然后用二甲胺处理。或者,与氯丙酰氯反应得到 1,3-双中间体,用二甲胺转化为氨基酮 3-(2-二甲氨基丙酰基)吲哚。用氢化铝锂将其还原为相同的产物 a,N,N-TMT。双马来酸盐的熔点为 139-140 °C。
苯丙胺世界和色胺世界之间存在另一个平行。与其在末端氮上添加第二个甲基,不如只保留现有的一个甲基,并将其延长一个碳原子。将甲基变成乙基。对于苯丙胺/甲基苯丙胺原型,这种延伸提供了同系物 N-乙基苯丙胺,并通过进一步延伸得到 N-丙基、N-丁基等苯丙胺。同样的操纵,再次在苯乙胺世界中,当芳香环上有 3,4-亚甲二氧基取代时,会得到 MDA、MDMA、MDE、MDPR 系列化合物。色胺领域也存在完全相同的世界。延长 a,N-DMT 的 N-甲基会导致在人类中已知且具有潜在活性的化合物,但尚未被探索。正如在 DET 下讨论的,色胺上存在两个不同的烷基时,最好以这两个基团命名,其位置以数字或字母作为首字母代码前的缀。但在这里,这种惯例变得极度模糊。如果其中一个前缀属于一个基团,而另一个属于另一个基团,该怎么办?当然必须把它们分开。但随后像 a-M-N-ET 之类的东西在长索引中很难正确定位。让我们折中一下,用 a-MET,其中 M 是 a 位,但 E(乙基)在色胺的 T 上,那是它所属的地方。因此,N-乙基化合物(alpha-甲基-N-乙基色胺)变成 a-MET,它来自吲哚-3-丙酮与乙胺的还原烷基化(盐酸盐熔点 187-189 °C,苦味酸盐熔点 203-205 °C),而 N-异丙基类似物(alpha-甲基-N-异丙基色胺)变成 a-MIPT,来自吲哚-3-丙酮与异丙胺的还原烷基化(盐酸盐熔点 229-230 °C,苦味酸盐熔点 219-220 °C)。它们在动物中的药理作用并不令人兴奋,但在人类中尚未尝试。好吧,也许尝试过。1962 年的一项早期专利给出了 N-甲基和 N-乙基化合物(a,N-DMT 和 a-MET)的合成方法,并声称它们都具有精神兴奋特性。
最后,作为一个注记,请小心。代码 TMT 有两种含义。在苯乙胺领域,它指的是麦司卡林类似物 3,4,5-三甲氧基反苯环丙胺(或反-2-(3,4,5-三甲氧基苯基)环丙胺)。这是 PIHKAL 的第 56 条,第 607 页,详情请查阅该处。在这里,多次甲基化的色胺条目(除了 DMT 之外的一个例外)将在代码前冠以甲基的具体位置,例如数字或希腊字母的前缀。