9. 右美沙芬的生理效应
这一节解释了目前关于右美沙芬及其生理效应的一些已知知识呢。由于对右美沙芬的娱乐性使用并没有得到很好的研究,这里的大部分信息都是推测,其中一些完全是我个人的看法。准确地说,很多内容都属于“科学瞎猜”(Scientific Wild-Assed Guessing,简称 SWAGging),大家看看就好,当作有趣且未被证实的假设哦。
这一章的很多内容非常硬核技术流。在下一章(第 10 节)中,你会看到神经药理学的介绍,词汇表(第 16 节)里也有这些技术术语的定义和解释。
9.1 右美沙芬如何抑制咳嗽反射?
这是个复杂的问题呢。咳嗽反射通常涉及一系列信号,起源于喉咙、肺部和鼻腔通道,最后到达肌肉。在这一路径的任何一点,信号都可能被阻断。Sigma 受体显然参与了这个路径 (42,49,55,56)。这可能是直接参与——Sigma 受体的激活可能直接抑制咳嗽反射信号——也可能是间接的。阿片类药物(如可待因)的镇咳效果与非阿片类吗喃衍生物(如右美沙芬)的镇咳效果并不相关 (49);相反,阿片类药物似乎是由传统的阿片受体(mu、kappa 或 delta)控制的。
有一些证据表明,5HT1A 受体(一种血清素受体)参与了这个路径的某个环节,并且镇咳药可能会增加 5HT1A 的活性 (57),这可能是通过 NMDA 拮抗作用实现的 (90)。这或许能解释右美沙芬的一些情绪改变活性。5HT1A 受体与焦虑状态和对厌恶事件的恢复能力有关。丁螺环酮(Buspirone)是一种 5HT1A 受体部分激动剂,它是一种抗焦虑药物,虽然效力不如苯二氮卓类药物如地西泮(Diazepam),但相当安全。
9.2 右美沙芬如何引起其精神活性作用?
如果你觉得咳嗽反射已经够复杂了,那是还没看到后面的呢!
9.2.1 常规信息
右美沙芬至少结合大脑中的四个位点 (58),我们可以随意地把它们标记为 DM1、DM2、DM3 和 DM4;可能还有第五个结合位点 (DM5)。 其中一些位点对喷他佐辛(一种已知的 Sigma 配体)敏感;有些对氟哌啶醇(另一种 Sigma 配体)敏感。 在下表中,我们收集并结合了来自多个来源的信息。列出了右美沙芬、DTG 和 3-PPP 的结合亲和力 (58),以及 (+)-喷他佐辛敏感性 (60) 和氟哌啶醇置换能力 (58)(除非另有说明,结合值以 nM 为单位)。“低”意味着微摩尔级的结合亲和力。
表 2:右美沙芬结合位点
| 右美沙芬位点: | DM1 | DM2 | DM3 | DM4 |
|---|---|---|---|---|
| 可能的结合位点: | Sigma1 | PCP2 | Sigma2 | NMDA |
| 右美沙芬 | 50-83 | 8-19 | 低 | 低 |
| (+)-3-PPP | 24-36 | 低 | 210-320 | 低 |
| DTG | 22-24 | ??? | 13-16 | ??? |
| 喷他佐辛敏感吗? | 是 | 否 | ??? | ??? |
| 氟哌啶醇可被置换吗? | 是 | ??? | 是 | ??? |
这个表格表明右美沙芬结合在四个不同的地方,其中两个具有高亲和力。基于与喷他佐辛和氟哌啶醇的结合以及 (+)-3-PPP 的效力,第一个受体被认为是 Sigma1 受体。鉴于对喷他佐辛的不敏感性以及对右美沙芬极高的亲和力,第二个受体几乎可以肯定就是 PCP2 受体。第三个位点 可能 是 Sigma2(基于 DTG 的效力),但也有可能表中的“DM1”代表了 Sigma1 和 Sigma2 两者,而第三个位点是别的什么东西。 第四个位点可能是 NMDA 受体的开放通道位点,尽管它也可能是离子通道结合位点 (59)。
遗憾的是,我没有关于右羟吗喃(DXO)结合情况的信息。它可能在 DM4(NMDA 开放通道位点)显示出最强的结合力,其次是 DM1(Sigma1),然后是 DM3(Sigma2)和/或 DM2(PCP2),或者两者兼有。我目前正在寻找这方面的信息呢。
9.2.2 PCP2 结合位点的作用
PCP2 结合位点可能就是多巴胺再摄取复合体,所以阻断它会阻止多巴胺的摄取,这与抗抑郁药安非他酮(Bupropion)或可卡因的作用方式非常相似 (73)。当然,右美沙芬在这个位点的作用比可卡因弱得多(顺便说一句,比安非他酮强)。 这可能解释了低剂量娱乐用药时的欣快感,而且几乎肯定解释了低剂量的兴奋作用。有趣的是,对于大多数人来说,这种兴奋效果似乎与苯丙胺(安非他命)有本质的区别(我没有关于可卡因的对比信息)。一位使用者认为右美沙芬在兴奋效果上比安非他酮更好。顺便提一下,右美沙芬似乎在多巴胺再摄取位点上是非竞争性结合,而安非他酮是竞争性结合。
音乐欣快感和运动欣快感可能部分归因于 PCP2 活性,部分归因于其他活性。由于 NMDA 阻断和 Sigma 活性都能导致多巴胺能活性(见下文),再摄取抑制会增强这些效果。
有趣的是,与其他 Sigma/NMDA 配体(如 PCP 或氯胺酮)相比,右美沙芬在这个位点的效力要强得多。同样有趣的是,至少有一种三环类抗抑郁药被发现对相关受体(Sigma, PCP)有活性 (71,74,75);这可能意味着 PCP2 位点可能是某些抗抑郁药的靶点。
9.2.3 Sigma 结合位点的作用
由于 Sigma2 位点是一个相当新的发现,目前还不知道哪些 Sigma 相关的效应和行为归因于哪个受体(Sigma1 或 Sigma2)。 关于 Sigma 配体的主观效应的数据非常少,部分原因是直到最近才有选择性配体可用,部分原因是大多数研究人员不太愿意拿自己当小白鼠来弄清楚。 右美沙芬结合 Sigma1 受体,通常被认为是该受体的激动剂。右美沙芬可能也是 Sigma2 的激动剂(相对于拮抗剂),尽管它在那里的作用要弱得多。
感官处理的中断可能部分归因于 Sigma 激活(部分归因于 NMDA 阻断)(63-65)。Sigma 受体可能专门参与右美沙芬的听觉效应 (65),这些效应可能与感官输入持续性的中断有关。
右美沙芬的拟精神病(字面意思是“像精神病一样的”)效应可能是 Sigma 活性的结果,因为 Sigma 受体似乎与精神分裂症有某种关联 (46-49)。既使用过右美沙芬又使用过氯胺酮的人评论说,右美沙芬更有可能诱发妄想和超抽象的思维模式。Sigma 受体可能会暂时调节胆碱能受体 (97),因此 Sigma 活性可能会产生类似于致妄想抗胆碱能药物的暂时效应。
对运动技能的影响可能具体是 Sigma2 受体的结果 (69)。随着对 Sigma2 受体的更深入研究,预计会有更多数据出现。当然,NMDA 受体也可能有贡献。
9.2.4 NMDA 受体的作用
右羟吗喃(DXO)在 NMDA 受体上的效力比右美沙芬强得多,这就解释了为什么即使注射右美沙芬,其大部分效应起效也很慢。NMDA 受体是解离作用的中心位点,可能是右美沙芬大部分效应的主要贡献者。解离剂,包括右美沙芬,通过在 NMDA 受体通道打开时结合并堵塞它来发挥作用。
右美沙芬的大部分“迷糊”或醉酒效应是由于 NMDA 受体阻断。酒精的醉酒效应似乎部分是由 NMDA 受体阻断介导的(酒精的抑制效应是由于 GABA 活性;右美沙芬在 GABA 受体上没有活性)(28,61,62)。 高剂量右美沙芬的解离性麻醉也可能是由于 NMDA 受体阻断 (63)。
如前所述,感官处理中断,特别是在较高剂量下,可能部分归因于 NMDA 受体,部分归因于 Sigma (63-65)。 NMDA 阻断可能导致了大部分(如果不是全部)右美沙芬的镶边效应,尤其是视觉镶边。这可能是一种间接效应,即 NMDA 受体的阻断诱导大脑处理信息的方式发生变化,从而导致镶边效应。
对记忆的影响几乎肯定也是由于 NMDA 阻断。 NMDA 受体与长时程增强作用(LTP)密切相关 (64,66-68),这是中时程记忆(ITM)和长时程记忆(LTM)背后的主要机制。通过阻断 NMDA 受体,长时程增强作用被破坏,从而干扰了中时程和长时程记忆的编码。
NMDA 阻断间接 (244) 增加了纹状体、伏隔核、嗅结节和前额叶皮层的多巴胺活性 (204,226,326)。 多巴胺 D1 受体活性的增加是大鼠在使用解离剂后运动活性增加的原因 (178),并且可能也是右美沙芬对运动产生的许多影响的原因。长期使用右美沙芬可能导致多巴胺 D2 受体的上调 (205)。
右美沙芬在中毒水平下抑制呼吸的能力最可能归因于 NMDA 受体阻断或(在我看来)离子通道阻断。非常高剂量下的一些效应可能是由于神经网络的整体中断。有一些初步证据表明,“自发记忆”效应和类似于濒死体验的感觉可能发生在边缘区域(海马体、海马结构及周围区域)被 NMDA 阻断破坏时。大多数药物针对特定的、小簇的神经元(或其受体,这些受体可能分散各处)。兴奋性氨基酸分泌神经元和 NMDA 受体倾向于分布得更均匀,尽管它们也在大脑的某些区域有一定程度的集中。
9.2.5 颞叶的参与
右美沙芬的大部分效应可能来自于上述受体结合对颞叶边缘区域造成的后果。右美沙芬对 NMDA 受体的阻断在这些区域有特定的后果。海马体和杏仁核的正常功能被破坏,因为 NMDA 阻断阻止了长时程增强作用。后扣带回和压后皮层反而变得更加活跃。整个边缘系统可能会有由反馈放大的自发“噪声”效应。一篇论文提出,解离剂可能在边缘系统诱发“微癫痫发作”或有限的高活性区域 (176)。
还有一种关于“自上而下”的感官抑制的说法,即来自边缘区域和周围皮层区域的抑制信号被“向下”发送到感官网络,降低感官数据的强度。这种“自上而下”的感官抑制可能是解离性麻醉背后的机制;感官信息仍然被大脑处理,但从未到达意识层面,也从未在中时程陈述性记忆(在海马体中)中编码。
最后,解离剂似乎改变了通过边缘区域的信号流,可能增加了这些区域内部(或这些区域与新皮层之间)的内部反馈程度,并减少了进入的感官数据量。与后扣带回的 Theta 节律耦合的信号门控 (311) 可能会被改变。
把所有这些整合成一个连贯的理论可能还为时过早,但我还是要试着说一下。我的信念(随着新研究的出现可能会改变)是,来自自上而下抑制的感官数据减少,以及中时程记忆编码的减少,加上后扣带回和压后皮层活性的增强,所有这些导致了一个日益封闭的反馈循环。 在这个循环中,随机噪声、颞叶“接线”的个体差异、中时程记忆的内容以及电磁场的影响 (332) 结合在一起,产生了极其异常的神经模式。
顺便提一个有趣的点,有时据报道右美沙芬会增强嗅觉。这还没有经过正式研究,可能完全是心理作用,但由于大脑处理嗅觉数据的方式与其他感官有些不同,它可能幸免于那些减弱其他感官数据的下行抑制信号。如果是这样的话,反馈循环实际上可能会通过反复叠加相同的微小信号来增强嗅觉数据的强度。
9.2.6 间接活动的贡献
右美沙芬的许多效应无疑归因于其他神经递质系统的间接活动。 例如,它可能间接增加 5HT(血清素)活性,特别是在 5HT1A 受体上。这可以解释它的一些情绪改变特性。另一个例子是多巴胺能活性;右美沙芬具有相当强的增加多巴胺活性的能力(既来自于激活 Sigma 受体,也来自于阻止 PCP2 位点的多巴胺再摄取)(72,76)。NMDA 受体阻断也被证明可以增加多巴胺能活性,以及其他神经递质系统的活性 (100)。
9.2.7 镶边效应
右美沙芬最显著的效应之一是感官输入的“镶边效应”(Flanging)。 这在某种程度上也发生在许多药物上,关于这一点我有一个假设。请特别注意镶边效应与“迷糊感”(stoning)和“嗡嗡感”(buzzing)的关系——在某些方面,镶边效应是一种更深程度的迷糊。有些人在吸食大量大麻后注意到镶边或频闪效应,氧化亚氮(笑气)使用者也熟悉声音的镶边。甚至酒精也能产生这种效果。
这许多药物的共同点似乎是能够抑制海马体的长时程增强作用(LTP)。有人建议,有多组信号通过相同的边缘区域,那些与 Theta 频率同相的信号和异相的信号会被不同的门控。也许一组信号与记忆更密切相关,另一组与感官数据更密切相关。或者,也许所有抑制海马体 LTP 的药物都会激活后扣带皮层。无论哪种情况,处于 Theta 节律某一相位的信号可能会被破坏,导致感知随 Theta 节律跳动。
另一种理论是,大脑中的网络会重复处理相同的数据,直到形成稳定的配置,而右美沙芬(和其他药物)会减慢这一过程。随着一些网络减慢而另一些以正常速度运行,两组信号的特征频率会有所不同,导致产生“拍频”,就像两个非常相似的声音会导致拍频一样(想快速演示这个,听听别人怎么用耳朵给吉他调音就知道了)。
9.2.8 超抽象
右美沙芬另一个有趣的效果是它能够引起奇特的认知障碍,我将其统称为“超抽象”。举两个例子:
- 模因(Meme) 是思想的“粒子”或“病毒”——一个在某种程度上自成一体并像病毒一样传播的想法。例如,公民自由的理念就是一个模因,它在某个时刻突然产生,迅速传播,现在已成为我们要意识的一个组成部分。一位使用者在右美沙芬旅程中突然意识到了(或者想到了)“自我调用、自我创造的模因”,这是一个其识别即创造并调用的模因概念。这个模因似乎是永恒的,因为它肯定一直存在,否则它就不会浮现在脑海中,因为它不容易从自身以外的任何事物推导出来(当然,大脑并不按逻辑规则运作,但是……你懂的)。
- 另一位用户写到了思考收敛的无穷级数(例如,1/2 + 1/4 + 1/8 + 等等,总和为 1)。虽然人们可以永远把这些项加下去,但抽象这个过程并以这种方式得到答案更容易。这位用户想象了一个无穷的抽象系列,然后想象抽象那个无穷系列以获得一个新的抽象水平或平面。
许多右美沙芬的思维模式涉及一些人所说的逻辑中的“怪圈” (137)。就像自相矛盾的陈述“这句话是假的”一样,其中一些无法以逻辑形式体现;另一些可以,但如果不作为假设提出就无法推导。在这种抽象程度上思考是非常困难的(除非你幸运地成为库尔特·哥德尔)。
几位写过关于精神病和精神分裂症第一人称叙述的人提到了日益抽象的思维模式(《禅与摩托车维修艺术》浮现在脑海中)。这当然可能完全是胡说八道,也许日益“抽象”的想法只是日益疯狂(因此难以与具体的想法联系起来)。另一方面,精神分裂症和精神病状态的某些方面可能与抽象层次之间的模糊有关。一旦足够模糊,一个无法在具体抽象程度上表现的想法就可以在脑海中表现出来。
因此,右美沙芬可能会诱发这种抽象层次的暂时模糊。这是由于 NMDA 还是 Sigma 活性,我不知道,尽管我怀疑是后者,因为其他 NMDA 拮抗剂往往不会引起这种思维模式的变化。
9.2.9 妄想和记忆问题
如上所述,Sigma 活性可能会调节大脑中的胆碱能受体 (97),导致胆碱能功能暂时下降,类似于阿托品、东莨菪碱、赛克利嗪(Marezine)等抗胆碱能药物引起的(但安全得多)效果。众所周知,胆碱能活性对记忆很重要,许多益智药(“聪明药”)都能增强胆碱能功能。Sigma 活性很可能导致某些胆碱能受体的有效性暂时降低,从而扭曲记忆和思维过程。事实上,有些人说右美沙芬让他们觉得自己暂时变笨了(有人要“笨蛋药”吗?),但这绝不是发生在每个人身上。
许多生物胺系统似乎具有调节作用,一些研究人员认为这些调节系统的运作方式很像“控制旋钮”。例如,关于 LSD 的一个理论是它扰乱了感官识别网络的“增益控制”(可能是通过下行抑制,尽管通过的途径与假设的解离剂途径不同)。 结果,随机噪声输入(任何模式匹配网络所必需的)变得比感官输入强得多。感官识别变得越来越不精确——这就是幻觉。
LSD 的效应几乎肯定比这更复杂,但关于生物胺系统的“控制旋钮”想法可能有一些道理。如果是这样,那么胆碱能系统可能是认知网络的“控制旋钮”,就像 5HT2A/5HT2C 系统是感官识别网络的控制旋钮一样。妄想可能只是幻觉的认知等价物。或者换句话说,认为你 看起来 像一朵花和认为你 就是 一朵花之间的区别可能在于哪个网络被破坏了。
记忆问题在某种程度上源于 NMDA 阻断,尽管一些氯胺酮使用者评论说右美沙芬对记忆的影响比氯胺酮更强。除了诱发妄想性思维外,胆碱能功能的下降也可能是造成某些记忆问题的原因。这当然与致妄想抗胆碱能药物的效应一致。
顺便说一句,抗胆碱能药物也会影响控制心脏和呼吸功能的乙酰胆碱受体(这些受体似乎不受 Sigma 活性调节)。抗胆碱能药物的娱乐性使用可能极其危险,导致呼吸衰竭或心力衰竭。
9.3 为什么右美沙芬表现出高原现象?
9.3.1 高原 1-3:多重受体
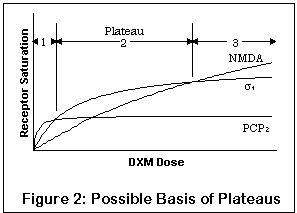 这张图说明了多重受体的潜在影响。
请注意,这是一个定性图,不是定量的;对于给定强度的右美沙芬,不同受体上的实际饱和度仍然大部分未知。线条代表 PCP2、Sigma1 和 NMDA 开放通道位点的饱和水平,曲线上特定受体的“变平”表示完全饱和。X 轴是右美沙芬的浓度;Y 轴是受体的饱和百分比。
这张图说明了多重受体的潜在影响。
请注意,这是一个定性图,不是定量的;对于给定强度的右美沙芬,不同受体上的实际饱和度仍然大部分未知。线条代表 PCP2、Sigma1 和 NMDA 开放通道位点的饱和水平,曲线上特定受体的“变平”表示完全饱和。X 轴是右美沙芬的浓度;Y 轴是受体的饱和百分比。
顺便说一句,如果你熟悉这类东西,你可能会更习惯林纳韦弗-伯克图(Lineweaver-Burk plot),但对于那些不熟悉的人来说,它们可能会令人困惑。
由于其对 PCP2、Sigma1 和 NMDA 受体的亲和力依次递减(Sigma2 未表示),低剂量将倾向于对 PCP2 受体产生比例更大的影响,而随着剂量的增加,这些受体将饱和。服用更多的右美沙芬不会改变 PCP2 水平太多,但仍会对其他受体产生相当大的影响。
此外,对 PCP2 受体的更微妙的影响可能会被 Sigma1 和 NMDA 受体的效用完全掩盖(三条曲线不同的垂直最大值代表了这种效应)。这是完全合理的,因为 Sigma1 和 NMDA 活性似乎都能产生相当深远的行为影响,后者比前者更甚。
因此,第一高原可能对应于主要是 PCP2 活性,伴有一些 Sigma 活性和一点点 NMDA 阻断效应;第二高原对应于 Sigma 和一些 NMDA 效应;第三高原对应于深刻的 NMDA 阻断。
当然,这是一种简化,它肯定没有考虑到受体的个体差异。有些人的受体可能有遗传变异,右美沙芬对其有更强(或更弱)的亲和力。一个 PCP2 受体被右美沙芬强力结合的人可能会比那些 PCP2 受体仅受微弱影响的人更享受其兴奋效果。
此外,这张图中省略了离子通道和 Sigma2 受体。它们无疑也有贡献,有些人断言在前三个高原之间还有其他高原。其中一些可能非常微妙,以至于大多数使用者都注意不到。
9.3.2 第四高原:感官关闭
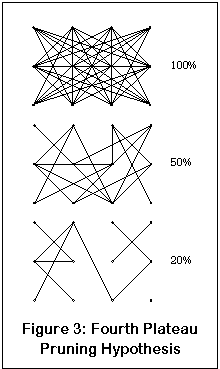
那第四高原呢?再一次,这是另一张希望能理清一切的小图(好吧,希望如此)。这张图代表了一个神经网络;点是神经元,线是它们的连接。像大脑的大部分一样,这个网络是高度互联的。百分比数字显示了剩余的功能链接数量。
当足够多的 NMDA 受体被阻断时,一个神经元可能会失去足够多的来自另一个神经元的输入,以至于连接实际上被切断了。 起初这并不是什么大问题,因为神经元和连接都足够密集,其他的可以接管工作(尽管最终结果可能是一个更慢、不太准确的网络)。 在某一点上,丢失了足够多的连接,网络就不再起作用了。
将此与第四高原的解离进行比较。在某种程度上,大脑的某些部分(可能是海马体)失去了足够的功能,以至于它不再能作为一个有凝聚力的单元运作。感官处理停止,原始感官输入无法转换为适当解析的输出。意识随后失去任何真实的感官输入;取而代之的是混乱、不稳定的模式。也就是,解离性麻醉。
另一方面,第四高原的阈值可能是当感官信息被抑制到足以让边缘区域的神经信号反馈而没有实质性地被感官输入“接地”时达到的。这个反馈循环继续扰乱神经信号模式,直到它们与人们可能从感官输入或记忆中遇到的任何状态完全断开连接。
9.4 为什么这这么复杂?
右美沙芬本身是一种非常复杂的药物;大多数药物只结合一个或两个受体(或至少一类受体)。虽然其娱乐滥用的潜力已被人们知晓多年,但并未得到很好的研究,它对不同人的影响可能有很大差异。它影响的受体和结合位点——Sigma、NMDA 和 PCP2——都是新发现。所有这些加起来就是一个复杂且知之甚少的药物。
此外,大脑本身是一个复杂的系统,我们对其功能仍然知之甚少。神经传递的基础似乎已被理解,但仍有许多问题。没有人知道为什么有这么多不同的神经递质,也不知为什么有这么多受体亚型。大多数受体的第二信使系统也没有被很好地理解。神经元内部发生的很多事情是通过基因表达的变化发生的,这又是另一个知之甚少的话题。
重复一句常被引用(且真实)的观点:如果这类大脑简单到我们容易理解,那我们就会简单到无法理解它们。我相信最终我们会对大脑的工作原理有一个很好的了解,但这可能不会在我有生之年实现。在此之前,我们都只是在摸黑瞎猜。
9.5 药代动力学:右美沙芬是如何代谢的
右美沙芬作为氢溴酸盐,从胃肠道吸收很快;在 30 分钟内,所有的右美沙芬可能都已经进入血液 (2,3)。聚苯乙烯磺酸(Polistirex)化合物旨在持续吸收,可能需要 6 到 8 小时才能完全进入血液。
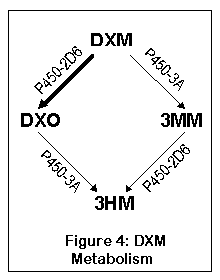
右美沙芬通过两条途径代谢,这两条途径都通向同一种东西,3-羟基吗喃(3HM)。 第一条途径是从右美沙芬到右羟吗喃(DXO),然后到 3HM;第二条是从 DXO 到 3-甲氧基吗喃(3MM),然后到 3HM。在正常个体中,绝大多数右美沙芬(高达 90%)通过 DXO 代谢。
右美沙芬通过一种叫做细胞色素 P450-2D6(德布里奎 4-羟化酶)的肝酶转化为 DXO。大约 7% 的白种人和 0.5% 的亚洲人拥有这种酶的高效能极低版本(慢 70 倍),无法有效地将右美沙芬代谢为 DXO (10)。大约 0.5% 到 2% 的人口拥有多个 P450 基因拷贝,导致右美沙芬极快地代谢为 DXO (155)。在转化为 DXO 后,酶 P450-3A4 和 P450-3A5 将 DXO 转化为 3-羟基吗喃 (77)。
另一条途径首先去往 3-甲氧基吗喃(通过 P450-3A4 和 P450-3A5),然后去往 3-羟基吗喃。大多数人不会以这种方式代谢太多的右美沙芬,尽管缺乏正常 P450-2D6 的人会将大量转化为 3MM。由于 3MM 可能没有精神活性,这意味着缺乏正常 2D6 酶的 5-10% 的人将体验到较少的右美沙芬效应(或者更具体地说,不会体验到 DXO 的效应)。
P450-2D6 的功能是去除甲氧基并用羟基 (OH) 代替(或者更准确地说,从氧上修剪掉甲基);这个步骤被称为 O-去甲基化。P450-3A4 和 3A5 用氢 (H) 代替甲基;这是 N-去甲基化步骤。请参考 第 4.2 节 中的右美沙芬分子图,了解甲基和甲氧基的位置。
9.5.1 影响右美沙芬代谢的因素
如上所述,有些人缺乏正常的 P450-2D6 酶。 在其余人群中,这种酶可能被几个因素抑制。许多药物会抑制 P450-2D6,特别是氟西汀(Fluoxetine,商品名百忧解)。第 15.1 节 给出了部分 P450-2D6 抑制药物的列表。
右美沙芬本身自然会与其他药物竞争 P450-2D6,重要的是,3-甲氧基吗喃(3MM)也会竞争 (17)。 事实上,3MM 对 P450-2D6 酶的亲和力可能比右美沙芬本身还要大。这可能解释了为什么第二剂“追加”(booster)剂量的右美沙芬通常会产生与第一剂不同的效果;对 P450-2D6 的竞争将减少第二剂中转化为 DXO 的右美沙芬量。
以下图表来自右美沙芬代谢的计算机模拟:
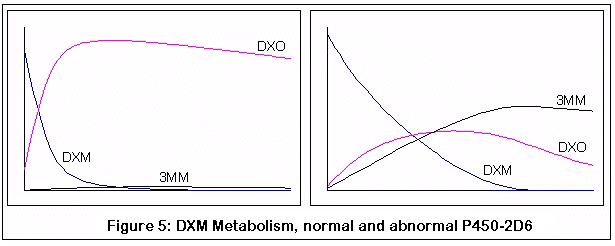
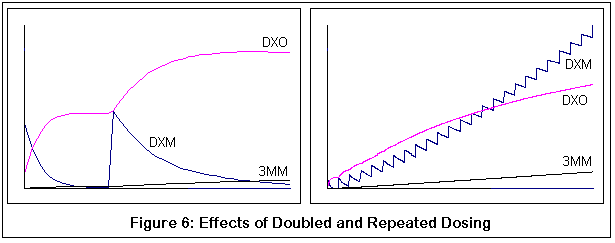
第一对代表了正常个体(左侧)和缺乏正常 P450-2D6 酶的个体(右侧)的右美沙芬代谢。注意正常个体中右美沙芬快速且几乎完全转化为 DXO,而缺乏 P450-2D6 的个体转化效率较低且较慢。
下一对展示了服用额外剂量(追加剂量)的可能结果。两个图表都对应于具有正常 P450-2D6 变体的个体。注意第二剂右美沙芬转化为 DXO 的速度没有那么快(因此斜率较浅)。 右侧图表显示了多次给药的情况,随着每一次给药,右美沙芬代谢曲线的“变平”越来越明显。
顺便说一句,这些是 定性 模拟,不是定量的。我试图遵守适用反应的已知 KM 和 VMAX 值,但模拟只是一个离散过程(老实说,我的微分方程技能已经生锈到如果你踩在上面就需要打破伤风针了)。我确实将我的结果与我就能找到的少量数据进行了比较,比较结果似乎是合理的,但也可能我完全偏离了基础。这些图表的目的是为了演示酶活性变化(通过遗传变异和 3MM 的竞争性抑制)的相对影响,希望这足以达到目的。
我没有关于 3-羟基吗喃本身会发生什么的信息。它可能由肾脏直接排泄,也可能经过进一步代谢。