10 右美沙芬的神经药理学
10.1 到底什么是受体?(基础神经药理学)
10.1.1 神经细胞的结构
所有的细胞在细胞外和细胞内之间都有一个电压梯度;如果你去测量细胞内外的电压,你会发现细胞内的电压比细胞外低大约 -100mV 呢。在大多数细胞中,这种电荷是离子泵入泵出细胞的结果,并没有什么特殊的用途。但是嘛,肌肉细胞和神经细胞会利用这种电荷哦。
肌肉细胞和神经细胞(神经元)拥有“可兴奋”的膜——也就是说,细胞膜两侧的电荷可以发生变化,而这种变化是有特定用途的。在神经元中,电荷的下降被用来传递信号。
人类大脑中有超过 100 亿个神经细胞,它们都在做同样的工作:将信号从输入端(树突)传递到输出端(轴突)。神经细胞看起来有点像一棵树,只不过它没有根和树枝,而是有树突和轴突。一般来说,树突接收信号,轴突传递信号(记住哦,信号是通过细胞膜电压的变化来表示的)。
在轴突的每个分支末端都有一个突触小体,这是一个类似按钮的小结构,用来向下一个神经细胞发送信号(稍后会详细介绍这个)。相反,树突用于接收信号,并且包含许多小凸起、旋钮之类的东西,每一个都接收来自另一个神经元的信号。一个神经元可能会接收来自成千上万个其他神经元的信号呢。
有些信号可能会兴奋细胞膜;另一些可能会抑制它。如果树突接收到的兴奋信号减去抑制信号的总和足够大,信号就会到达神经细胞体(胞体)。一旦胞体接收到足够强的信号,它就会沿着轴突发送出去并进行传输。
这就是神经元个体运作的基础啦。但是,这并没有解释一个神经元是如何向另一个神经元发送信号的(反过来说,它们是如何接收信号的)。极少数神经元是物理连接在一起的,信号就像微芯片里的信号从一个晶体管传到另一个晶体管一样,直接从一个细胞传到另一个细胞。然而,大多数神经元并不相互接触;相反,它们通过称为神经递质的化学物质进行交流,并利用称为神经受体的结构来接收它们。
10.1.2 神经传递
受体是位于细胞表面或内部的一种结构。如果在神经细胞(神经元)上,它通常被称为神经受体。受体的存在是为了接收来自特定化学物质的信号,当它们接收到这些信号时,通常会对细胞的功能产生某种改变。有些受体存在于细胞内部,被称为胞内受体;许多类固醇(睾酮、雌激素等)的受体就是胞内受体哦。
因为这一章是关于神经药理学的,所以重点将放在神经受体上,也就是文中简称为受体的东西。神经受体存在于神经细胞表面(或者较少见的情况下,在内部),并对称为神经递质的化学物质做出反应。有些神经递质也作用于神经细胞以外的细胞;例如,乙酰胆碱激活肌肉细胞上的受体,告诉它们收缩。
神经递质像钥匙插进锁里一样嵌入受体,而且一般来说,不会嵌入任何其他受体。因此我们有乙酰胆碱(一种神经递质)和乙酰胆碱受体。有些受体(称为离子通道受体)被激活时会刺激或抑制膜电位(从而影响神经细胞的活动);其他的(代谢型受体)会引起细胞特性的改变。有些离子通道受体(钙通道)可以两者兼得呢。
一般来说,神经细胞上的受体位置是为了接收来自另一个神经细胞的信号。树突当然有受体,但受体也可以存在于细胞体、轴突或突触小体上。两个神经细胞之间的“接口”被称为突触。
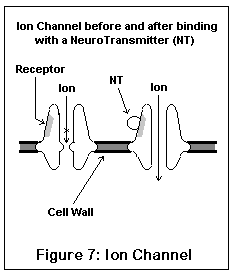
离子通道神经受体通常运作得非常快,作用(和外观)有点像照相机的光圈快门。神经递质(例如乙酰胆碱)结合到通道上的特定区域,这(由于静电力)导致通道猛地打开。特定的离子随后渗入和渗出神经细胞,改变其电位。不同的通道允许不同的离子通过;有些离子(如钠离子)兴奋神经细胞,其他的(如钾离子和氯离子)抑制它。一旦神经递质离开受体,通道就会猛地关上,完成了它的工作。这些是参与快速信号传输和传递骨骼肌脉冲的受体哦。
代谢型受体具有调节作用。它们中的一些会增加或减少其他类型受体的数量。有些会引起细胞内基因表达的改变。有些(称为自身受体)会抑制其自身匹配神经递质的释放,这个过程称为负反馈。恒温器就是负反馈系统的一个例子——天气越热,炉子开得越少。一般来说,这些较慢的受体通过第二信使(在细胞内充当信使)如 G 蛋白来运作。
任何给定的神经递质可能与几种不同的受体相关联。例如,5-羟色胺(5HT)至少激活十二种受体亚型(5HT1A、5HT1B、5HT1D、5HT1E、5HT1F、5HT2A、5HT2C、5HT3、5HT4、5HT5、5HT6 和 5HT7)!之所以有几种亚型(而不是只有一种),是因为每种受体亚型在不同类型的神经元上参与不同的过程。
药物通过以某种方式影响神经传递来作用于大脑。有些药物刺激受体,有些阻断受体;有些会改变神经递质的分泌、降解或回收方式。在很大程度上,药物起作用只是因为它们影响了现有的神经递质系统;尽管流行的观点认为变得“嗨”等同于烧坏脑细胞,但让你“嗨”的药物只是通过模仿、阻断或以其他方式影响神经传递来做到这一点的呢。
模仿、阻断或以其他方式影响特定神经递质活动的药物不会同等地影响所有受体亚型。例如,LSD 作用于 5HT2A 和 5HT2C 受体;丁螺环酮作用于 5HT1A 受体。因此,它们有非常不同的效果;LSD 是致幻的,而丁螺环酮是一种抗焦虑药物。
不同的物质可能结合到同一个受体但对其产生不同的影响。激动剂是一种结合受体并激活它的物质。部分激动剂是一种不能完全激活受体的激动剂。拮抗剂结合受体并阻止其运作。
部分激动剂的一个有趣特性是它们倾向于“正常化”受体活动水平。在神经递质含量低的情况下,部分激动剂会增加受体功能。然而,在神经递质含量高的情况下,部分激动剂会限制受体活动;实际上,许多拮抗剂实际上可能是部分激动剂呢。关于 LSD 是 5HT2C 拮抗剂还是部分激动剂仍有争议。
拮抗剂可能结合到神经递质结合的同一个地方,从而与神经递质“竞争”——这些被称为竞争性拮抗剂。或者它们可能结合到受体复合物上的另一个地方,这样即使神经递质到达其结合位点,受体也不会激活。这些被称为非竞争性拮抗剂。请注意,无论哪种情况,药物的结合都只是暂时的;如果是永久性的(从而有效地破坏受体),那就是不可逆拮抗。
竞争性和非竞争性拮抗剂之间的重要区别在于:如果你用竞争性拮抗剂阻断受体,只要分泌足够多的神经递质,这些受体仍然可以被神经递质激活。然而,如果你用非竞争性拮抗剂阻断受体,无论多少神经递质都无法激活该受体(直到非竞争性拮抗剂消失)。
可以用一个相当异想天开的类比来描述神经递质的功能和马桶的关系。在这种情况下,马桶是受体,你是神经递质,通过按下冲水把手来激活它。如果你弟弟跑过来帮你冲了厕所,他就是激动剂。如果他暂时把把手卡在一半,那就是部分激动剂。如果他把把手拉住不让你冲,那就是竞争性拮抗剂。如果他拿厕纸把马桶堵住了,那就是非竞争性拮抗剂哦。如果他把把手彻底掰断了,那就是不可逆拮抗剂啦。
生物胺神经递质(之所以这么叫是因为它们属于胺类化学物质)包括乙酰胆碱、去甲肾上腺素、多巴胺、5-羟色胺(5HT)和组胺。它们来源于氨基酸(分别为胆碱、酪氨酸、酪氨酸、色氨酸和组氨酸),通常具有调节作用,并且是娱乐药物的常见目标。例如:LSD、DMT 和裸盖菇素针对 5HT 受体;苯丙胺引起多巴胺和去甲肾上腺素的释放;可卡因阻断多巴胺的重摄取(从而使其活性保持更长时间);MDMA 引起 5HT 和多巴胺的释放;等等。娱乐药物及其神经受体活性的主要列表在第 15.2 节给出。
神经肽神经递质包括一大堆肽(氨基酸链),如神经肽 Y、血管紧张素、内啡肽、P 物质等等。针对神经肽受体的唯一娱乐药物是阿片类药物,它们针对 mu、kappa 和 delta 阿片受体。阿片受体(显然)参与疼痛和行为强化。加压素,一种益智药(“聪明药”),也是一种肽类神经递质。
氨基酸神经递质包括GABA(γ-氨基丁酸)、谷氨酸和天冬氨酸。这些神经递质的受体包括 GABA 受体(主要有两种口味)和 NMDA、AMPA(以前称为使君子氨酸)、红藻氨酸和代谢型受体(所有这些都对谷氨酸和天冬氨酸有反应)。GABA 受体是苯二氮卓类药物如地西泮(安定™)、巴比妥类药物和酒精的目标;NMDA 受体是 PCP、氯胺酮、酒精和右美沙芬的目标。
然后还有那些不太适合归类的受体。大麻素受体是最近发现的大麻中 THC 的目标。腺苷受体倾向于抑制神经活动,被咖啡因阻断(通过这种方式发挥其兴奋作用)。Sigma 受体最初被归类为阿片受体,但现在被认为是独立的。γ-羟基丁酸,GHB,似乎也针对特定的受体。
每个受体可以有一个以上的结合位点(药物可以结合的地方,通常影响受体的活性)。例如,NMDA 通道/受体复合物有七个(谷氨酸、甘氨酸、镁离子、锌离子、PCP 开放通道位点、多胺位点和磷酸化位点)。大多数受体的位点比这少;NMDA 通道是一个极其复杂的受体呢。
电压依赖性离子通道类似于快速域、像快门一样的受体,除了它们是由细胞膜两侧的电压电位打开的。它们通常沿神经纤维传递信号,或导致轴突末端释放其神经递质。钠、钾、钙和氯(Na+、K+、Ca2+ 和 Cl-)是通常涉及的离子。河豚毒素,“僵尸粉”中的活性成分,是一种钠通道阻滞剂。NMDA 受体具有电压依赖性离子通道的一些特征(见下文)。
10.2 什么是 Sigma 受体?
Sigma 受体发现于 1976 年(Sigma 通常用希腊字母写——σ——如果你的网络浏览器能显示那个,那你比我幸运),目前是神经药理学中最令人困惑的实体之一。比起我们的无知,我们对 Sigma 受体的了解简直微不足道;事实上,我们绝对知道的(或者至少认为我们绝对知道的)可以用下面这段话简要概括:
在整个大脑和身体中散布着一些地方(Sigma 结合位点),一堆化学物质(Sigma 配体)碰巧会粘在那里。我们不知道它们是在细胞外面还是里面。我们不知道把化学物质粘在上面会不会起什么作用,除了在输精管里。我们真的不知道它们是做什么的,如果它们真的做什么的话。我们不知道它们是为了什么,为什么在那里,或者身体是否使用它们。它们可能是神经受体、类固醇受体、细胞内信使受体、生长调节剂、酶,或者完全是别的什么东西。
换句话说,做好被绕晕的准备吧喵。别担心,其他人也都晕着呢。
Sigma 受体最初被认为是阿片受体,因为许多吗啡衍生物结合在那里 (283)。然而,这种分类可能是错误的,内源性阿片肽显示出很少的 Sigma 活性。阿片类药物的通常特征是由 mu (μ)、kappa (κ) 和 delta (δ) 受体介导的。至少有两个 Sigma 受体,第三个(很恰当地称为 Sigma3)最近也被发现了 (114)。
一些研究人员推测 Sigma 受体根本不是受体,而只是酶结合位点 (84)。另一方面,Sigma 配体影响豚鼠输精管肌肉,这在 Sigma 受体不是真的受体的情况下可能不会发生 (97)。Sigma 受体可能是为了激素或细胞内信使而不是神经递质,因为它们存在于微粒体而不是细胞表面 (129)。
10.2.1 Sigma 1 受体和一般 Sigma 信息
关于 Sigma 受体的大部分已知信息似乎更多地适用于 Sigma1 而不是 Sigma2(尽管这绝不是普遍的)。我将以下信息归类为 Sigma1 受体,但不要把它当作绝对真理哦。我预计很多最终会被证明是错误的。幸运的是,我们可能不需要等太久;Sigma 受体的研究正在迅速进行。
10.2.1.1 内源性配体
Sigma1 受体的神经递质尚未找到,尽管有一些推测和证据 (82-86,98-99)。对于(未识别的)Sigma1 神经递质的通常术语是“Endopsychosin”(内源性精神素)(99),以前称为“Angeldustin”(天使尘素)。孕酮针对胎盘中的 Sigma1 受体,它和其他类固醇激素可能是 Sigma1 受体的天然配体 (97,102,103)。如果是这样的话,性激素对大脑的一些影响可能是由 Sigma1 受体介导的 (97)。P 物质(一种肽类神经递质)被考虑过但被拒绝作为内源性 Sigma1 配体 (111)。DHEA 可能是一种 Sigma1 激动剂,而孕酮是一种拮抗剂 (258)。
10.2.1.2 大脑中的位置和功能
Sigma 受体在小脑皮层 (281)、伏隔核和皮层中密度最高,在边缘区域和锥体外系运动系统中也以较低密度存在 (260)。这很有趣,因为右美沙芬对运动的一些奇怪影响可能与小脑皮层和锥体外系运动系统中的 Sigma 活动有关呢。
Sigma1 受体(可能还有 Sigma2)似乎在功能上与其他一些受体偶联,特别是烟碱乙酰胆碱受体 (97,116) 和 NMDA 受体 (106-109,275)。它们实际上可能位于 NMDA 受体上或附近 (222)。
烟碱受体偶联可能是直接的,Sigma 激活引起烟碱受体功能的改变。至于调节烟碱受体是否会改变尼古丁对大脑的影响,我不知道;有些人在使用右美沙芬期间表示烟草会引起强烈的反应。
Sigma 激动剂(也可能还有拮抗剂)似乎影响记忆功能,逆转由药物如对氯苯丙胺和 MK-801(一种类似于氯胺酮的药物)引起的记忆损伤 (130,131)。DTG、(+)-喷他佐辛和 SKF-10047 都改善了由 MK-801 引起的记忆损伤。另一方面,被认为是 Sigma 拮抗剂的 NE-100 似乎也有助于缓解 NMDA 拮抗剂引起的记忆损伤 (106-107)。DTG,一种 Sigma 激动剂,逆转了一氧化碳引起的记忆损伤 (117)。
现在被认为是 Sigma 拮抗剂或激动剂的许多药物实际上可能是部分激动剂。另一种可能性是 Sigma 活动的最佳水平可能是一个健康的中间值;一项研究发现 Sigma 激动剂有钟形曲线剂量反应 (117)。这类似于许多益智药(聪明药)的效果,特别是胆碱能药物——吃太多可能比完全不吃还要糟糕。这种相似性可能是 Sigma 受体和乙酰胆碱受体之间联系的进一步证据。
Sigma1 激动剂和拮抗剂都可以保护 NMDA 受体免受谷氨酸毒性 (108)。一项研究发现 Sigma 拮抗剂保护海马细胞免受缺氧和低血糖的影响 (104),这也可能与 NMDA 受体有关。吗啡对 NMDA 受体有间接影响,似乎是通过 Sigma 受体介导的,可能是 Sigma1 (109)。所有这些效应都有可能是通过烟碱受体介导的,即 Sigma1 可能不直接控制 NMDA 功能。
10.2.1.3 行为影响
Sigma1 受体的行为影响尚未完全确定。然而,Sigma1(和 Sigma2)受体似乎对运动功能有影响,产生运动增加 (112,113,120)。这种影响的一部分可能发生在小脑 (112);多巴胺的释放也可能参与其中 (113,128)。这可能是右美沙芬对动作和步态的奇怪影响的起源,包括“晕船腿”和“Robo 拖步 (Robo Shuffle)”。
Sigma1 激活可能会抵消阿片类药物的一些镇痛作用 (118)。喷他佐辛(Talwin),一种合成阿片类药物,是一种强效的 Sigma1 激动剂,往往具有自限性;当服用过多时,Sigma 活性会逆转阿片活性 (267)。有可能吗啡和海洛因使用者经历的欣快感逐渐丧失可能与 Sigma 活性引起的变化有关。
Sigma 受体似乎参与了来自精神分裂症和药物的拟精神病(字面意思是“类似精神病”)效应 (46-49)。苯丙胺精神病,一种因大量使用精神兴奋剂而导致的暂时状况,可能部分归因于 Sigma1 活性 (80,125)。Sigma,特别是 Sigma1 受体,可能会被精神分裂症改变。正在研究的另一种可能性是某种化学物质——由身体本身产生,或由病毒或其他外来因子产生——导致 Sigma 受体的长期激活,而这就是精神分裂症的原因之一 (47,49)。许多抗精神病药,包括一些非典型抗精神病药,都是 Sigma 拮抗剂 (47,260)。一些抗抑郁药也是 Sigma 拮抗剂,并且都会最终减少 Sigma 结合 (260)。甲基苯丙胺会增加 Sigma 结合 (211)。
Sigma 受体可能参与松果体的功能,松果体是一个分泌褪黑激素(维持“生物钟”)的内分泌腺。Sigma 活性调节去甲肾上腺素刺激的松果体褪黑激素合成 (256),实际上松果体内也有 Sigma 受体 (266)。
除了右美沙芬,其他娱乐药物如 PCP、可卡因和阿片类药物都在 Sigma 受体上显示出活性 (72)。长期使用苯丙胺会增加 Sigma 受体的数量 (80),而长期抗抑郁和抗精神病治疗会减少 Sigma 受体的数量 (47,74)。Sigma 受体参与大脑的边缘区域 (81),因此可能参与情绪。它们也参与咳嗽反射,并且可能参与癫痫发作(或至少是预防发作)。
10.2.1.4 身体中的位置和功能
Sigma1 受体也存在于全身各处。大多数肿瘤细胞表达 Sigma1 和 Sigma2 受体 (38,105),Sigma 激动剂可以抑制肿瘤生长 (269)。肝脏和肾脏细胞也包含 Sigma 受体 (123),心脏细胞 (124) 和脾细胞 (274) 也是如此。如上所述,胎盘包含 Sigma1 受体。
Sigma 受体也存在于免疫系统和内分泌腺中,并可能负责调节这些系统。Sigma 激动剂可以通过调节 T 细胞来防止移植组织的排斥反应 (263)。有一些证据表明 Sigma 激动剂可能抑制免疫系统。Sigma 受体的广泛存在可能表明其参与发育、细胞调节或其他基本生物过程。
10.2.2 Sigma 2 受体
关于 Sigma1 受体的大部分说法可能也适用于 Sigma2 受体。还没有太多时间来区分这两种受体类型。Sigma2 受体的神经递质可能是锌离子 (78),Sigma2 受体似乎与钾离子通道有关 (79)。Sigma2 受体受右美沙芬的影响小于 Sigma1 受体 (58)。一些 Sigma 诱导的 NMDA 功能增强可能是由于 Sigma2 受体 (116)。伊博格碱,目前正在测试作为海洛因成瘾的治疗方法,是一种 Sigma2 激动剂 (273,283)。也发现了其他 Sigma2 受体的配体 (261,265,268)。
一项研究发现,长期接触 Sigma 配体,无论是激动剂还是拮抗剂,都会导致脑细胞退化和死亡 (101)。这种恶化表现为细胞形状的逐渐丧失;细胞最终变成球形(并在不久后死亡)。有趣的是,一些药物,包括右美沙芬,似乎在这种效果上非常微弱。虽然氟哌啶醇在几小时内引起显著变化和细胞死亡,但右美沙芬需要 3 天才能产生任何变化,并且在去除右美沙芬后这些变化会逆转。不同 Sigma 配体的效力似乎指向 Sigma2 受体是这种效应的罪魁祸首。
顺便说一句,我不会太担心这个。诱导任何变化所需的右美沙芬浓度非常高,而且需要持续接触 3 天。所有的变化都是可逆的,即使在细胞已经变成球形之后。氟哌啶醇和其他 Sigma 配体在产生脑细胞退化方面似乎比右美沙芬强 100 倍,但在医学上使用时并没有实质性的脑损伤证据。最后,如果存在足够水平的类固醇激素,很可能也会引起同样的效果(这也是不使用合成类固醇的另一个原因吧)。
10.2.3 Sigma 3 受体
Sigma3 受体是一个新发现 (114)。它们似乎与酪氨酸转化为多巴胺有关,Sigma3 激动剂可能会增加多巴胺合成的速率。右美沙芬在 Sigma3 受体上的效力未知,但如果它在那里结合强烈,那么增加的多巴胺合成可能是右美沙芬兴奋作用的部分原因。已经发现了一些 Sigma3 配体 (262)。
10.3 什么是 NMDA 受体?
10.3.1 NMDA 和其他谷氨酸受体
大多数更广为人知的神经递质系统——特别是多巴胺、去甲肾上腺素、5-羟色胺 (5HT) 和乙酰胆碱——具有调节作用。它们由位于特定簇中的少数神经元产生,影响它们的药物通常具有特定的效果(娱乐或医疗,或两者兼而有之)。这些神经递质的受体往往运作相当缓慢,需要毫秒或更长时间来交流。它们通常不是直接改变神经元的电位,而是经常触发第二信使反应。
另一方面,大脑的大部分常规功能运作迅速,涉及兴奋性和抑制性氨基酸(分别为 EAA 和 IAA)。氨基酸的受体通常是离子通道;当受体被激活时,离子进入或离开细胞,改变其电位。EAA 和 IAA 突触通常对应于电子和计算机神经网络中的正和负突触连接。
兴奋性氨基酸神经递质包括谷氨酸和天冬氨酸。GABA 是大脑中唯一确定的抑制性氨基酸神经递质;脊柱也使用甘氨酸。一般来说,谷氨酸比天冬氨酸更突出(或者至少被理解得更好),尽管它们在 EAA 受体上有类似的效果。因此,EAA 的受体被称为谷氨酸受体。
目前有四种已识别的谷氨酸受体类型。其中两种,AMPA(以前称为使君子氨酸)和红藻氨酸受体,是离子通道受体,它们响应 EAA 增加神经元活动。第三种,代谢型谷氨酸受体,是一个较新的发现,似乎涉及第二信使系统并产生代谢效应。第四种是 NMDA 受体。
10.3.2 NMDA 受体结构和功能
这幅画代表了根据当前知识的 NMDA 受体结构。
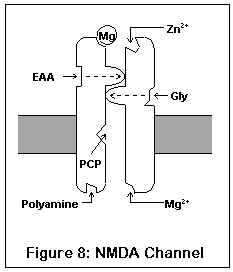
NMDA 受体有七个不同的结合位点。其中三个位于细胞的外表面,两个位于细胞内部,一个位于通道内部,还有一个(镁离子位点)存在于内外表面。
细胞外有两个激动剂位点,标记为 EAA 和 Gly;它们对应于兴奋性氨基酸(谷氨酸和天冬氨酸)和甘氨酸。在这两个位点都被占据之前,通道无法打开足够的程度让任何离子通过。第三个位点是锌离子 (Zn2+) 的目标,当锌离子存在时会阻断通道。
通道外部包含一个镁离子位点。这个位点也存在于细胞内部(或者,它可能位于通道本身内部)。在生物条件下,一个镁离子通常占据外部位点;内部位点可能是空的。
细胞内部包含两个结合位点。一个结合多胺(精胺和亚精胺),其功能未知。另一个,图中未显示,是磷酸化位点。酶可以结合到这个位点并增强或减少受体的活性。
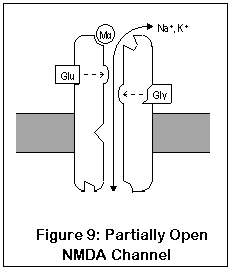
最后,在通道本身内部是 PCP1 位点,PCP、氯胺酮、MK-801(地佐环平)、右美沙芬和右啡烷都结合在这里。通道必须完全打开才能让这些药物进入;一旦就位,它们就会“堵塞”通道。
NMDA 受体之所以独特有几个原因。与大多数受体不同,它们需要两种激动剂(谷氨酸或天冬氨酸,加上甘氨酸)才能打开通道。这两种激动剂(图中的 Glu 和 Gly)结合到 NMDA 受体上的两个不同位置。在这两种激动剂都结合到通道后,它打开到足以让钾进入,受体的运作很像 AMPA 和红藻氨酸受体。如图 9 所示。
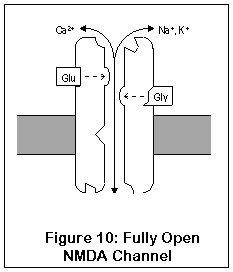
然而,NMDA 受体最重要和最独特的特征是接下来发生的事情(图 10)。通常,一个镁离子结合在通道开口处的特定位置;这个离子允许钾通过但阻止钙,可能是由于其大小。这种结合是由于静电力。
然而,一旦细胞变得足够活跃,细胞电位上升到一定程度,镁离子就不再粘在细胞上了。钙可以通过完全打开的 NMDA 通道进入(和离开,虽然这不会发生)细胞。一旦进入内部,钙就会启动一系列反应,增强突触的强度。
那么这有什么意义呢?嗯,如果神经元只是稍微活跃,NMDA 通道可能会部分打开,但镁离子没有机会离开其结合位点。然而,如果神经元被迅速或大量激活,镁离子就会被释放,钙就可以进入细胞,增强突触强度。这个增强突触强度的过程称为长时程增强 (LTP),是神经元改变其功能和“学习”的机制之一。海马体中的 LTP 可能负责短期记忆。学习能力实际上可能直接与海马体(被认为是存储中期记忆的地方)中的 NMDA 受体数量有关 (88)。LTP 是可逆的,长期记忆似乎是通过基因表达和突触形状的更永久性变化来存储的。
NMDA 受体双重作用的另一个有趣方面是它充当一种“巧合探测器”。只有当膜电位足够低并且突触被激活时,钙才会进入细胞;因此它探测突触信号和细胞内信号何时重合。在联想网络(海马体似乎就是这样的)中,NMDA 受体的构造理想地帮助神经元“学习”两个输入信号之间的关联。
至少有三种类型的 NMDA 受体(至少在大鼠中是这样;这可能也适用于人类)。一种类型发现于小脑,一种在丘脑,一种在皮层。这些类型有微妙的不同,但有可能右美沙芬对这些类型的影响谱可能与其他 NMDA 拮抗剂(如氯胺酮或 PCP)不同 (87)。也有一些推测认为 NMDA 受体的离子通道可能(由于未知原因)与受体本身“解偶联” (63)。
已知开放通道阻滞剂对 NMDA 受体的非竞争性拮抗会在整个大脑中引起变化。NMDA 阻断导致中脑和前额叶皮层中多巴胺释放增加 (63)。NMDA 阻断也导致专门针对 5HT1A 受体的 5HT 系统的激活 (90)。
10.3.3 NMDA 受体和兴奋性毒性
NMDA 受体参与兴奋性毒性(通过过度刺激导致的神经细胞死亡)。激动(激活)NMDA 受体的化学物质也可以杀死它们正在激活的同一个神经细胞 (19)。许多物质,如喹啉酸(色氨酸的代谢产物)是如此强效,以至于极少量就能摧毁大量的神经细胞。其他的,如谷氨酸和天冬氨酸,效力较低,但如果存在足够的量仍能造成损害。这种兴奋性毒性直接导致了归因于各种类型的创伤和中枢神经系统损伤的大部分损害。脊髓灰质炎就是一个很好的例子;通过阻断喹啉酸的活性,可以防止脊髓灰质炎造成的所有损害 (30-31)。右美沙芬并不是一种特别有效的 NMDA 开放通道阻滞剂,但右啡烷、PCP、氯胺酮和 MK-801(地佐环平)都是非常有效的阻滞剂。
不幸的是,生活里从来没有免费的午餐哦。降低的 NMDA 活性,称为 Olney 病变、NMDA 受体功能减退 (NRH) 或 NMDA 拮抗剂神经毒性 (NAN),似乎本身也要对其他神经元的兴奋性毒性负责。该理论认为正常的 NMDA 活动可以防止其他神经递质(谷氨酸和乙酰胆碱,可能还有多巴胺)被过度分泌。NMDA 阻断解除了这种抑制,因此可能导致某些神经元的过度活跃。慢性 NMDA 阻断可能是精神分裂症和阿尔茨海默病的原因,或者至少是一个因素 (100)。
娱乐水平的 NMDA 阻断尚未得到充分研究,Olney 病变仅在远超娱乐水平的剂量下出现。我的直觉是,偶尔的 NMDA 阻断可能对大脑并没有太大的创伤;否则,John Lilly 肯定比现在笨多啦。特别是右美沙芬可能更安全,因为它在 NMDA 受体上的效力较低,并且 Sigma 活性可能具有抵消作用。更多信息请参见第 6.3.1 节。
最后一点说明:婴儿可能对这种效应特别敏感,因此在怀孕或哺乳期间使用任何 NMDA 拮抗剂可能都是个坏主意 (112)。甚至有人认为胎儿酒精综合症部分是由 NMDA 阻断的影响介导的。
10.4 什么是 PCP2 受体?
PCP2 受体显然是第二个被确定的 PCP 受体(第一个是 NMDA 受体上的开放通道位点)。它们在体内的用途(如果有的话)尚未确定。大多数研究表明 PCP2 受体是多巴胺重摄取复合物,与可卡因和哌甲酯(利他林™)以及可能还有抗抑郁药安非他酮(威博隽™)所针对的是同一个 (70,126)。
顺便说一句,重摄取复合物(或重摄取位点)是细胞上的一种结构,它将用过的神经递质带回细胞进行回收或分解。通过阻断神经递质的重摄取,可以增加其活性。三环类抗抑郁药阻断去甲肾上腺素、多巴胺和/或 5-羟色胺 (5HT) 的重摄取。氟西汀(百忧解™)是一种 5-羟色胺特异性重摄取抑制剂 (SSRI),其他几种较新的抗抑郁药也是如此。多巴胺重摄取位点似乎是唯一被娱乐药物(主要是可卡因)针对的重摄取位点。
奇怪的是,安非他酮,一种多巴胺重摄取抑制剂,似乎没有什么娱乐用途潜力;不过话又说回来,它并不是一种特别强的多巴胺重摄取抑制剂。有人建议它是一种竞争性重摄取抑制剂,因此只能抑制少量多巴胺的重摄取。大量的多巴胺会压倒竞争性抑制的效果。
10.5 什么是 Na+ 和 Ca2+ 通道?
钠离子和钙离子通道是两种类型的电压依赖性离子通道。这些通道的开启或关闭不是由于神经递质,而是由于细胞内外的电压差。
电压依赖性钠通道通常参与动作电位——神经冲动沿轴突的多米诺骨牌效应传播。当电压达到某个激活阈值时,钠通道打开;随之而来的钠内流进一步激活神经元(导致更多钠通道打开)。最终,钠通道的第二部分关闭(否则它们会永远保持开放)。顺便说一句,电压依赖性钾通道参与将神经元带回其静息状态。
电压依赖性钙通道类似于电压依赖性钠通道,通常在激活电压下打开。然而,它们的作用是让钙进入细胞;钙随后充当细胞内机制的信使。最常见的例子是在轴突末端,钙内流导致神经递质被释放。NMDA 受体可能在结构上与电压依赖性钙通道有关。
已发现右美沙芬可以阻断钠和钙通道,尽管它在这方面的效力并不是特别强。由于它们的广泛存在,阻断这些离子通道可能对大脑功能产生整体抑制作用,并且可能解释右美沙芬在非常高剂量下的毒性作用。
10.6 在这些受体上,右美沙芬与其他解离剂相比如何?
PCP 和氯胺酮都比右美沙芬更强地结合到 NMDA,而在 PCP2 和 Sigma 位点上结合得较弱。事实上,一些用户报告说,右美沙芬在较高剂量下开始类似于氯胺酮和 PCP。相似之处仍然相当有限。右美沙芬的独特特征很可能是由于 PCP2 和 Sigma 位点。
10.7 内源性精神素和宏观图景
不管出于什么原因,有些从事生物科学的人喜欢谈论“宏观图景”。我就是其中之一。我认为“宏观图景”之所以看起来如此重要,是因为科学,特别是生物科学,已经变得如此专业化和条块分割,以至于很难保持全局视角,特别是当考虑到事物的可能相关性时。
Endopsychosin(内源性精神素,发音:en-doe-sy-KOE-sin)是赋予 NMDA 开放通道位点 (PCP1) 和/或 Sigma 受体的内源性配体的名称。寻找内源性精神素始于几年前,旨在寻找 PCP 的内源性配体;当时,这个术语是“angeldustin”(天使尘素)。最近,随着 NMDA 和 Sigma 受体越来越被理解,寻找内源性精神素的工作又重新开始了。在我写这篇文章的时候,还没有人能确定一种内源性精神素,尽管有几个候选者。NMDA PCP1 位点最有希望的候选者似乎是一系列肽 (98-99)。Sigma1 位点的内源性配体可能是一种未知的芳香族化学物质 (97,99)。
内源性精神素(如果你喜欢的话,也可以叫天使尘素)背后的最初想法是,身体能够分泌一种物质来模仿 PCP 对大脑的影响。它可能在极端压力下分泌,导致一种超然的、梦幻般的感觉。内源性精神素可能负责诸如宗教狂喜、说方言、附身、星体投射和其他超自然体验等意识改变状态。内源性精神素的自发释放可能解释了诸如外星人绑架、遇到鬼魂之类的事情。另一方面,这些状态可能更好地用颞叶复杂部分性癫痫发作或其他电学故障来解释。
注意这些体验与右美沙芬、氯胺酮和 PCP 药物旅程方面的相似之处。特别是,与氯胺酮相关的“涌现现象”(也存在于 PCP 和右美沙芬中)通常包括与精神或外星生物的体验。
这是怎么回事呢?为什么人类大脑会分泌一种化学物质,让我们以为我们在火星背面和猫王还有 Jim Morrison 聊天?宏观图景是什么?
嗯,老实说,没人知道。一个潜在的线索是海马体的穿通通路(一种神经回路)在受到刺激时似乎会释放内源性精神素 (138)。也许内源性精神素是记忆过程的一部分;或者也许它参与了做梦以及中期记忆向长期记忆的转化。另一个建议是内源性精神素参与长时程抑制 (LTD),即长时程增强的反面。
另一种可能性是内源性精神素是大脑抵御伤害的自然防御之一。我觉得有趣的是,Sigma/NMDA 药物经常模仿发烧幻觉;共同特征包括小人国幻觉、几何和线性幻觉以及烦躁不安。也许大脑在高烧期间分泌内源性精神素是为了防止神经毒性。
除了潜在的神经保护作用外,这些物质可能在调节认知和(在体内)免疫和内分泌系统中具有重要作用。内源性精神素或 Sigma 受体(或两者)的功能障碍可能是精神分裂症的原因之一。如果一些类固醇(例如孕酮和睾酮)被证明是内源性精神素,这可以解释很多关于使用类固醇的长期行为影响。
或者,仅仅是因为意识改变状态是动物生命的自然组成部分,而我们的文化对这种状态的恐惧是不正常的。当然,不需要药物就能达到意识改变状态;即使是深刻的解离状态也可以通过一定量的仪式和信仰来达到。大多数“原始”文化都有一些解离状态的经验,如星体投射、萨满之旅、附身之类的。他们可能真的很清楚一些我们不知道的事情。
最后,内源性精神素(以及模仿它们的药物)的感知效果可能仅仅是边缘系统中发生的更基本事情的副作用。也许这些外星人和精神遭遇以及其他超自然现象(见第 8 节)是有意识的头脑解释通常不会进入意识的边缘网络状态的方式。
所以完全有可能 NMDA PCP1 和 Sigma 受体之间的相似性是有目的的。无论如何,关于 Sigma 特异性激动剂(或拮抗剂)影响的数据是有限的,但随着研究的继续,我们对这些受体的理解应该会在未来几年内提高。更不用说可能有一些勇敢和/或愚蠢的精神探索者决定尝试 Sigma 特异性激动剂。
(+)-3-PPP 和 SKF-10,047 是好的 Sigma 特异性配体;更多 Sigma1 特异性配体包括 1-苯基环烷羧酸衍生物 (122,127)。有人觉得勇敢吗?也许你可以成为下一个 Shulgin(有人想要写一本《我所认识和喜爱的内源性精神素》吗?)。不过话又说回来,也许你最好不要;你要是得了什么治不好的疯病,我可不想被起诉呢。