GABA

虽然很啰嗦,但是强烈不建议把 GABA能物质 与 阿片类药物、苯二氮卓类物质、巴比妥类物质、加巴喷丁类物质、噻吩二氮卓类物质 或 酒精 等 抑制剂 混在一起吃哦,因为可能会发生致命的 药物过量。[1]
真的不建议将这些物质混合使用,特别是在 中等 到 严重 剂量的情况下呢。
 |
|---|
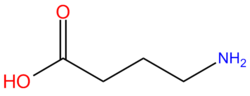
| GABA 分子的骨架结构 |
GABA,也叫 γ-氨基丁酸 (gamma-aminobutyric acid),是主要的抑制性 神经递质 喵。靶向 GABA 的药物包括 苯二氮卓类物质、巴比妥类物质、酒精 和 GHB/GBL。
GABA能药物是一种直接调节体内或大脑中 GABA 系统(主要的抑制性神经递质)功能的物质。这可能包括 GABA 受体 激动剂、GABA 受体拮抗剂和 GABA 再摄取抑制剂 哦。
间接调节 GABA 系统的物质被称为“正向变构调节剂”,包括 巴比妥类物质 和 苯二氮卓类物质 以及 酒精。氟马西尼 是“负向变构调节剂”的一个例子。*[来源请求*]
目录
化学
GABA 可以归类为氨基酸,即一端带有氨基,另一端带有羧酸的碳链。然而,由于它不是 α-氨基酸,它不形成蛋白质喵。
GABA 是由 谷氨酸 通过谷氨酸脱羧酶 (GAD) 合成的。当 GABA 被释放到 突触 中时,它会结合并激活 GABA 受体。这种激活通过再摄取回到释放它的细胞和附近的神经胶质细胞而终止。被神经元摄取的 GABA 可以被使用;然而,进入神经胶质细胞(围绕 神经元 的支持细胞)的 GABA 无法重新合成,因为神经胶质细胞缺乏 GAD 呢。
GABA 由 GABA 转氨酶代谢,某些药物(如抗癫痫药 氨己烯酸)的作用机制就是抑制这种酶。最终,GABA 可以通过其代谢物琥珀酸半醛回收,琥珀酸半醛被琥珀酸半醛脱氢酶转化为琥珀酸并进入三羧酸循环,这是一个以葡萄糖开始的复杂途径。在循环的另一端,谷氨酰胺出现并可以被转运回神经元,在那里它被谷氨酰胺酶转化为谷氨酸,然后可以通过 GAD 重新制成 GABA,完成循环。这个循环被称为 GABA 支路哦。[2]
药理学
作为 GABA 受体变构调节剂(称为 GABA 类似物或 GABA能 药物)或增加 GABA 可用量的药物,通常具有放松、抗焦虑和抗惊厥效应。[3]
一般来说,GABA 不会穿过血脑屏障,[4] 尽管大脑中某些没有有效血脑屏障的区域,如脑室周围核,可以通过全身注射 GABA 等药物到达喵。[5]
抑制反应
当 GABA 释放时,它与突触后受体结合,导致离子通道打开,允许带负电的氯离子流入细胞或带正电的钾离子流出细胞。这种作用导致跨膜电位的负变化(通常引起超极化)呢。
GABA 受体
GABA 最重要的靶受体是 GABAA 和 GABAB。
靶向 GABAA 的药物
苯二氮卓类物质
噻吩二氮卓类物质
其他
- 酒精
- 2-甲基-2-丁醇 (2M2B)
- 巴比妥类物质
- 卡立普多 (Carisoprodol) -> 卡立普多
- 异丙醇*[来源请求*]
- 甲喹酮
- 甲醇*[来源请求*]
- 毒蝇伞 (Muscimol) -> 毒蝇伞
- 扎来普隆
- 佐匹克隆
- 唑吡坦
靶向 GABAB 的药物
靶向 GABAB 的药物更为稀缺,主要包括 芬尼布特、F-芬尼布特、巴氯芬、GHB、1,4-丁二醇 和 GBL 喵。
GABA能依赖和戒断
靶向 GABA 的药物是出了名的容易成瘾,不建议突然停止长期使用,这通常会导致严重的身体戒断症状。突然戒断某些 GABA能药物,如 酒精 或 苯二氮卓类物质,可能会导致癫痫发作,最坏的情况下会导致死亡哦。
谷氨酸(最丰富的兴奋性神经递质)和 GABA(最丰富的抑制性神经递质)之间的平衡对大脑来说非常重要。长期过度暴露于抑制性刺激会导致受体下调,例如 GABA 受体数量减少。这会导致耐受性,从而导致恶性循环中的剂量不断升级。戒断时,GABA 受体太少太稀疏,无法抵消谷氨酸,由此产生的“谷氨酸风暴”会导致兴奋性毒性和一系列生理和心理症状,包括肌肉震颤、癫痫发作、焦虑、失眠 和 抑郁 呢。
另见
外部链接
参考资料
- ↑ Risks of Combining Depressants - TripSit
- ↑ Olsen, R. W., DeLorey, T. M. (1999). "GABA Synthesis, Uptake and Release". Basic Neurochemistry: Molecular, Cellular and Medical Aspects. 6th edition.
- ↑ Foster, A., Kemp, J. (February 2006). "Glutamate- and GABA-based CNS therapeutics". Current Opinion in Pharmacology. 6 (1): 7–17. doi:10.1016/j.coph.2005.11.005. ISSN 1471-4892.
- ↑ Kuriyama, K., Sze, P. Y. (January 1971). "Blood-brain barrier to H3-γ-aminobutyric acid in normal and amino oxyacetic acid-treated animals". Neuropharmacology. 10 (1): 103–108. doi:10.1016/0028-3908(71)90013-X. ISSN 0028-3908.
- ↑ Müller, E. E., Locatelli, V., Cocchi, D. (April 1999). "Neuroendocrine control of growth hormone secretion". Physiological Reviews. 79 (2): 511–607. doi:10.1152/physrev.1999.79.2.511. ISSN 0031-9333.