169 2-TOET
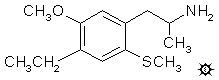
4-ETHYL-5-METHOXY-2-METHYLTHIOAMPHETAMINE 4-乙基-5-甲氧基-2-甲硫基苯丙胺
 |
|---|
合成: 将 24.4 g 邻乙基苯酚和 18.9 mL 碘甲烷的混合物加入到 15.6 g 85% 氢氧化钾溶于 100 mL 热甲醇的溶液中。混合物保持回流温度过夜,尽可能除去甲醇,并倒入 1 L 水中。加入过量的 5% 氢氧化钠,用 3x75 mL 二氯甲烷提取。合并提取液用 1% 氢氧化钠洗涤,真空去除溶剂,得到 32.8 g 淡琥珀色油状物。将其在 55-65 °C (0.4 mm/Hg) 下蒸馏,得到 22.0 g 2-乙基苯甲醚,为无色油状物。
向 21.7 g 搅拌良好但无溶剂的 2-乙基苯甲醚样品中,一次 1 mL 地加入 21 mL 氯磺酸。颜色从白色变为黄色,最后变为深紫色,并释放出大量氯化氢。允许放热反应混合物搅拌直至恢复至室温(约 0.5 小时)。然后在良好的机械搅拌下将其倒在 400 mL 碎冰上,产生大量淡粉色固体。过滤去除,用水充分洗涤,风干得到约 27 g 3-乙基-4-甲氧基苯磺酰氯,为保留一些水分的米白色固体。用环己烷重结晶的样品熔点为 44-46 °C。用氢氧化铵处理的样品产生 3-乙基-4-甲氧基苯磺酰胺的白色晶体,可用水重结晶得到一簇簇晶体,熔点 97-98 °C。分析 (C9H13NO3S) C,H。
在配备机械搅拌器的 2 L 圆底烧瓶中,加入 200 mL 碎冰、45 mL 浓硫酸、26.7 g 仍湿润的 3-乙基-4-甲氧基苯磺酰氯和 45 g 元素锌粉。外部加热引发放热反应,并保持回流条件 4 小时。冷却至室温后,过滤反应混合物,不溶物交替用水和二氯甲烷洗涤。母液和洗涤液用足够的水稀释,使二氯甲烷成为下层。分离各相,水相用 3x100 mL 二氯甲烷提取。合并原始有机相和提取液,用水洗涤,去除溶剂得到 15.7 g 有臭味的琥珀色油状物。将其在 72-84 °C (0.3 mm/Hg) 下蒸馏,得到 12.1 g 3-乙基-4-甲氧基苯硫酚,为水白色油状物。红外光谱完美(SH 伸缩振动在 2562,OCH3 在 2837 和 1061,指纹峰在 806, 880, 1052, (1061), 1142 和 1179 cm-1)。分析 (C9H12OS) C,H。
向 11.7 g 3-乙基-4-甲氧基苯硫酚和 6.5 mL 碘甲烷溶于 100 mL 甲醇的溶液中,在良好搅拌下分次加入 5.5 g 85% 氢氧化钾溶于 25 mL 热甲醇的溶液。混合物在蒸汽浴上回流 1.5 小时,然后在真空下除去挥发物。残留物加入到 400 mL 水中,用 5% 氢氧化钠强碱化,并用 3x75 mL 二氯甲烷提取。合并提取液用 1% 氢氧化钠反洗,真空去除溶剂。蒸馏 13.2 g 残留物,得到 2-乙基-4-(甲硫基)苯甲醚,沸点为 78-85 °C (0.2 mm/Hg)。重量为 11.6 g,分离产率超过理论值的 90%。熔点约为 0 °C。红外光谱未显示 SH 或其他官能团,但在 2832 和 1031 处有 OCH3,指纹谱峰在 808, 970, (1031), 1051, 1144 和 1179 cm-1。分析 (C10H14OS) C,H。
用 13 g 无水氯化铝分次处理 11.2 g 2-乙基-4-(甲硫基)苯甲醚和 9 g 二氯甲基甲醚溶于 200 mL 干燥二氯甲烷的溶液。颜色从粉红色变为紫红色,再到深紫红色,伴随适量氯化氢释放。继续搅拌 1 小时,然后通过小心加入 250 mL 水来淬灭反应。两相混合物再搅拌一小时然后分离。水相用 2x100 mL 二氯甲烷提取。合并有机相,用 5% 氢氧化钠洗涤,然后用饱和盐水洗涤,真空去除溶剂。残留物为琥珀色油状物,重 13.7 g。在 0.2 mm/Hg 下蒸馏。第一馏分为黄色油状物,沸点 90-100 °C,重 2.9 g。它是起始苯甲醚和所需苯甲醛的混合物。第二馏分沸点 100-130 °C,为粘稠黄色油状物,重 4.8 g。经薄层色谱分析,它不含起始苯甲醚,并含有相当数量的第二种苯甲醛。从该馏分中获得晶种,当油状物溶解于等体积甲醇中时,晶种起作用,产生黄色固体。过滤并风干,得到 2.2 g 4-乙基-5-甲氧基-2-(甲硫基)苯甲醛,熔点 62-63 °C。来自甲醇的小样品几乎是白色的,熔点 61-62 °C。与 4-乙基-2-甲氧基-5-(甲硫基)苯甲醛(57-58 °C)的混合熔点严重降低(37-44 °C)。蒸馏第一馏分的甲醇溶液冷却后提供额外的 1.6 g 产物,熔点 59-61 °C。合并母液得到额外产物,总重 5.3 g。分析 (C11H14O2S) C,H。
将 1.9 g 4-乙基-5-甲氧基-2-(甲硫基)苯甲醛溶于 75 mL 硝基乙烷的溶液用 0.3 g 无水乙酸铵处理,并在蒸汽浴上保持 2.5 小时。真空去除过量的溶剂/试剂,残留的深橙色油状物溶解于 10 mL 沸腾的甲醇中。冷却时,自发生成晶体。在冰浴中冷却几小时后,过滤去除,用甲醇洗涤,风干至恒重。共获得 1.4 g 1-(4-乙基-5-甲氧基-2-甲硫基苯基)-2-硝基丙烯,为金丝雀黄晶体,熔点 83-84 °C,经甲醇重结晶未见改善。分析 (C13H17NO3S) C,H。
向 1.5 g 氢化锂铝溶于 30 mL 无水四氢呋喃的溶液中(冷却至 0 °C 并在氦气下搅拌),缓慢加入 1.05 mL 新制备的 100% 硫酸(通过向 1.0 g 96% 浓硫酸中加入 0.9 g 20% 发烟硫酸制备)。随后在 10 分钟内加入 1.4 g 1-(4-乙基-5-甲氧基-2-甲硫基苯基)-2-硝基丙烯溶于 20 mL 四氢呋喃的溶液。加入后硝基苯乙烯溶液的颜色立即消失。继续搅拌,使其恢复至室温,然后温和回流 2 小时。再次冷却至室温后,加入异丙醇破坏过量的氢化物。加入足够的 5% 氢氧化钠以生成松散可过滤的无机盐块,将其过滤去除。滤饼用额外的异丙醇充分洗涤,合并母液和洗涤液在真空下去除溶剂。残留物溶解于 100 mL 稀硫酸中,用二氯甲烷洗涤,用 5% 氢氧化钠碱化,并用 2x75 mL 二氯甲烷提取。去除溶剂得到残留物,在 102-117 °C (0.15 mm/Hg) 下蒸馏。蒸馏出的无色液体 (0.7 g) 溶解于 6 mL 异丙醇中,用 11 滴浓盐酸中和。形成的固体通过短暂加热混合物至沸腾而溶解,此澄清溶液用 20 mL 无水乙醚稀释。4-乙基-5-甲氧基-2-甲硫基苯丙胺盐酸盐 (2-TOET) 的白色晶体,重 0.6 g,熔点 164-167 °C。分析 (C13H22ClNOS) C,H。
给药剂量: 大于 65 mg。
药效时长: 未知。
定性评论: (摄入 50 mg)大约一个半小时后,我发现自己有点头重脚轻。也许还有一种身体有点脆弱的感觉。我吃了一些东西,但吃东西并没有多少乐趣。第二天还有一些残留的脆弱感,不管那意味着什么。谨慎前行。
(摄入 65 mg)白天这几乎不明显,但很愉快。
延伸和评论: 似乎硫在 2 位时比在 5 位时更无趣,效力也更低。2-TOM 需要 5-TOM 两倍的剂量,而这里看来可能需要 5-TOET 两倍的剂量才能让 2-TOET 起效。当身体不适感超过精神作用时,对于推高新未知化合物的剂量有一种可以理解的不情愿。这里没有任何实质性的东西。在 50 毫克试验的完整报告中,提到无法勃起,加上头重脚轻和对食物不感兴趣,都表明交感神经系统受到了一些牵连。由于这些微妙的影响持续到第二天,为什么要推高剂量呢?直觉说别管它。所以我没管它。
2-碳类似物,2C-2-TOET,是由相同的醛中间体制成的。相应的硝基苯乙烯由醛和硝基甲烷顺利制得,从甲醇中得到闪亮的南瓜橙色晶体,熔点 93-94 °C。分析 (C12H15NO3S) C,H。最终的苯乙胺盐酸盐是通过在四氢呋喃中用氢化铝还原制备的,并以常规方式分离。它是一种白色结晶块,熔点 226-227 °C。它与 TOM 和 TOET 的其他 2-碳类似物一样,目前仍未品尝。