9 ASB
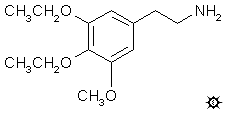
不对称麦司卡林;3,4-二乙氧基-5-甲氧基苯乙胺
 |
|---|
合成:向32 g 5-溴乙基香兰素的150 mL 二甲基甲酰胺溶液中加入31 g 碘乙烷和32 g 精细研磨的85% 氢氧化钾颗粒。形成了紫色并产生大量沉淀。逐渐加热至回流,颜色褪色为浅黄色,沉淀在1小时内溶解。继续加热1小时。将反应混合物加入1 L 水中,用2x150 mL 石油醚萃取。合并萃取液,用2x200 mL 5% 氢氧化钠洗涤,最后用水洗涤。经无水碳酸钾干燥后,在真空下除去溶剂,得到36 g 粗制的3-溴-4,5-二乙氧基苯甲醛,为琥珀色液体。这步产物未经纯化直接用于下一步。在0.3 mm/Hg、105-115 °C下蒸馏得到白色样品,未结晶。分析数据:(C11H13BrO3) C,H。
将36 g 3-溴-4,5-二乙氧基苯甲醛和17 mL 环己胺的混合物用明火加热,直到看起来不含水。残余物置于真空(0.4 mm/Hg)下,在135-145 °C下蒸馏,得到42 g 3-溴-N-环己基-4,5-二乙氧基苯亚甲胺,为粘稠的浅绿色油状物。这缓慢凝固成结晶玻璃状,熔点为60-61 °C。从己烷中重结晶得到白色结晶产物,熔点没有提高。分析数据:(C17H24BrNO2) C,H。这是一种利用可用的溴原子合成许多活性碱的化学中间体。该溴原子可以被硫原子交换(导致5-TASB和3-T-TRIS)或被氧原子交换,如下所述。
将18 g 3-溴-N-环己基-4,5-二乙氧基苯亚甲胺的250 mL 无水乙醚溶液置于氦气氛围中,磁力搅拌,并用外部干冰/丙酮浴冷却。然后在2分钟内加入36 mL 1.5 M 丁基锂的己烷溶液,产生透明的黄色溶液。搅拌10分钟。然后一次性加入30 mL 硼酸丁酯,继续搅拌5分钟。让搅拌后的溶液恢复至室温。加入150 mL 饱和硫酸铵水溶液。分离乙醚层,水相用另外75 mL 乙醚萃取。合并有机相,真空蒸发。残余物溶解在100 mL 甲醇中,用20 mL 水稀释,然后在2分钟内加入15 mL 35% 过氧化氢处理。让这个轻微放热的反应搅拌15分钟,然后加入500 mL 水。用2x100 mL 二氯甲烷萃取,真空除去溶剂。残余物悬浮在150 mL 稀盐酸中,在蒸汽浴上加热0.5小时。继续搅拌直到反应再次达到室温,然后用2x75 mL 二氯甲烷萃取。合并这些萃取液,用3x100 mL 稀氢氧化钾水溶液萃取。水萃取液用二氯甲烷洗涤,用盐酸重新酸化,并用2x75 mL 二氯甲烷重新萃取。合并这些萃取液,真空除去溶剂,得到棕色残余物。在0.4 mm/Hg、107-127 °C下蒸馏,得到8.3 g 3,4-二乙氧基-5-羟基苯甲醛,为凝固成棕褐色固体的油状物。从环己烷中重结晶得到白色产物,熔点为70.5-71.5 °C。分析数据:(C11H14O4) C,H。
将8.3 g 3,4-二乙氧基-5-羟基苯甲醛和3.0 g 氢氧化钾在75 mL 乙醇中的溶液用5 mL 碘甲烷处理,并在室温下搅拌5天。将反应混合物加入400 mL 水中,并用2x50 mL 二氯甲烷萃取。合并萃取液,用2x150 mL 稀氢氧化钠洗涤,真空除去溶剂。残余油状物在0.3 mm/Hg、95-110 °C下蒸馏,得到8.2 g 3,4-二乙氧基-5-甲氧基苯甲醛,为浅黄色液体。该产物在20 °C以下为结晶固体,但在恢复至室温时熔化。对其进行了分析,并作为油状物用于进一步反应。分析数据:(C12H16O4) C,H。
向6.4 g 3,4-二乙氧基-5-甲氧基苯甲醛的40 mL 硝基甲烷溶液中加入约0.5 g 无水乙酸铵,回流1小时。真空除去过量的溶剂/试剂,产生凝固成晶体的红色油状物。将其从40 mL 沸腾的甲醇中重结晶,得到3.0 g 3,4-二乙氧基-5-甲氧基-β-硝基苯乙烯,为黄色片状物,熔点为89-90 °C。分析数据:(C13H17NO5) C,H。
将3.0 g 氢化铝锂在150 mL 无水四氢呋喃中的溶液在氦气下冷却至0 °C并剧烈搅拌。在10分钟内滴加2.1 mL 100% 硫酸,随后滴加3.5 g 3,4-二乙氧基-5-甲氧基-β-硝基苯乙烯的30 mL 无水四氢呋喃溶液。添加过程是放热的。混合物在蒸汽浴上回流30分钟。再次冷却后,用异丙醇破坏过量的氢化物,随后加入足够的10% 氢氧化钠,将氧化铝转化为白色颗粒状。通过过滤除去,用异丙醇洗涤滤饼,合并母液和滤液,真空除去溶剂,得到黄色油状物。将该残余物加入100 mL 稀硫酸中,产生浑浊的悬浮液和一些黄色不溶性胶状物。用2x75 mL 二氯甲烷洗涤。水相用25% 氢氧化钠调至碱性,并用2x75 mL 二氯甲烷萃取。从这些合并的萃取液中除去溶剂,残余物在0.4 mm/Hg、110-135 °C下蒸馏,得到2.0 g 无色液体。将其溶解在7 mL 异丙醇中,用约40滴浓盐酸中和,随后在搅拌下加入50 mL 无水乙醚。最初透明的溶液自发析出白色结晶固体。用另外30 mL 乙醚稀释,静置1小时,过滤除去固体。经乙醚洗涤后,产物空气干燥,得到1.25 g 3,4-二乙氧基-5-甲氧基苯乙胺盐酸盐(ASB),熔点为142-143 °C。分析数据:(C13H22ClNO3) C,H。
给药剂量:200 - 280 mg。
药效时长:10 - 15 小时。
定性评论:(240 mg剂量)有一种愉快而轻松的白日梦思绪流,非常友好且带有一点色欲。到午夜时分(我早上9:00开始),我的心理状态温和地回落到了初始基线。我从未完全达到+++,对此感到相当遗憾。
(280 mg剂量)效果的平台期在第二小时就很明显了,但我发现这次体验缺乏我所希望的视觉和解释性的丰富感。在效果基本消退后,睡眠非常不安稳——很难躺下并放松警惕——甚至在第二天四处走动时,我仍感到残留的“+1”效应。总的来说,几乎没有2C-B或LSD那种开放的互动感。似乎存在一些负面影响。
(280 mg剂量)整个过程在某种程度上就像是在一个走廊里,外面是灯火通明的礼堂,那里正在进行着美丽的麦司卡林体验,能感觉到灰色门后传来的光,却无法从昏暗的地下通道中找到进去的路。这算是麦司卡林的一种温和的姐妹,但倾向于强调(对我来说,在那个时候)负面的、悲伤的、挣扎的一面。十五小时前无法入睡。当我尝试入睡时,我看到了沙漠中的月光幻象,周围的人影是灵魂的吸血鬼-狼人化身,颜色发绿且邪恶。我不得不静静地坐在客厅里,耐心地等待它们退回到属于它们的地方,停止尝试接管画面。在体验的高峰期,我的脉搏细弱,有些缓慢且不齐。有一种微弱的身体上的怪异感。
延伸和评论:多年前在荷兰,曾对猫进行过一次针对这种特定胺的研究,使用的是从巴塞尔的罗氏制药获得的材料。他们的发现很难评估,因为给一只3.75公斤的猫注射了200毫克(53 mg/Kg),大约是他们在对位麦司卡林研究中所用剂量的两倍。5分钟内出现了木僵迹象,半小时内动物无法行走。这种情况持续了两天,此时动物死亡。虽然这个剂量是人类剂量的许多倍,但也许可以从中收集到身体不适和药效持久的暗示。超过六次实验的共识是,它的价值不足以抵消所经历的身体负荷。
需要对这个奇怪的名字“asymbescaline(不对称麦司卡林)”做一个评论!在奇妙的化学命名世界中,bi-(或di-)通常意味着两个某物,而tri-和tetra-很合理地意味着三个和四个某物。但偶尔bi(或tri或tetra)可能会产生歧义,因为bi-某某可能意味着两个某某连接在一起,或者可能是两个东西连接在一个某某上。所以,前者被称为bi-,后者被称为bis-。这种化合物不是两个麦司卡林连接在一起(bi-escaline),而是只有一个麦司卡林,上面附着了两个乙基(bis-escaline,简称bescaline)。既然有两种方式可以做到这一点(对称或不对称),对称的那个被称为symbescaline(简称SB),而这个被称为asymbescaline(简称ASB)。为了完成术语讲座,术语tri-变成了tris-(给予所有三个甲氧基都被乙氧基取代的麦司卡林类似物的名称),而术语tetra-则变异成了相当不可思议的tetrakis-!