29 2C-G-4
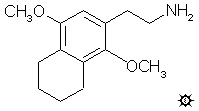
2,5-二甲氧基-3,4-(四亚甲基)苯乙胺; 6-(2-氨基乙基)-5,8-二甲氧基-四氢萘
 |
|---|
合成: 向49.2 g 5,6,7,8-四氢萘酚(5-羟基四氢萘)溶于100 mL甲醇的溶液中,加入56 g碘甲烷,随后加入24.8 g氢氧化钾颗粒(85%纯度)溶于100 mL沸腾甲醇的溶液。混合物在55 °C浴中加热3小时(约10分钟出现第一批白色碘化钾固体)。真空除去溶剂,残留物溶于2 L水中。用盐酸酸化,并用4x75 mL二氯甲烷萃取。有机相用3x75 mL 5%氢氧化钠洗涤后,真空除去溶剂,得到48.2 g黑色残留物。将其在0.25 mm/Hg下于80-100 °C蒸馏,得到33.9 g 5-甲氧基-1,2,3,4-四氢萘,为白色油状物。氢氧化钠洗涤液经酸化和二氯甲烷萃取,真空除去溶剂并蒸馏残留物(0.35 mm/Hg)后,得到11.4 g回收的起始苯酚。
将61.7 g三氯氧磷和54.3 g N-甲基甲酰苯胺的混合物在蒸汽浴上加热15分钟,产生深红色。将其加入54.3 g 5-甲氧基-1,2,3,4-四氢萘中,混合物在蒸汽浴上加热2小时。在剧烈搅拌下将反应混合物淬灭于1.2 L水中。生成的油状物迅速变成棕色颗粒状固体,过滤除去。将79 g湿产物在等重量的甲醇下精细研磨,过滤,用20 mL冰冷甲醇洗涤,并风干得到32.0 g 4-甲氧基-5,6,7,8-四氢萘甲醛,为象牙色固体。滤液静置后,又沉积出4.5 g产物,将其加入上述第一批中。通过乙醇重结晶获得分析样品,熔点为57-58 °C。分析元素(C12H14O2):C,H。
向25.1 g 4-甲氧基-5,6,7,8-四氢萘甲醛溶于300 mL二氯甲烷的溶液中,以与放热反应相称的速度加入25 g 85%间氯过氧苯甲酸。几分钟内出现固体。搅拌的反应混合物回流加热8小时。冷却至室温后,过滤除去固体,并用二氯甲烷轻微洗涤。合并滤液和洗涤液,真空除去溶剂,残留物溶于100 mL甲醇,并用40 mL 25%氢氧化钠处理。在蒸汽浴上加热一小时,加入1 L水中,并用盐酸酸化,产生大量结晶块。过滤除去,风干,并在高达170 °C、0.2 mm/Hg下蒸馏。从而得到21.4 g 4-甲氧基-5,6,7,8-四氢萘酚,为灰白色固体,熔点为107-114 °C。通过70%乙醇重结晶获得分析样品,熔点为119-120 °C。己烷也是极好的重结晶溶剂。分析元素(C11H14O2):C,H。作为替代方法,可以通过在含有过氧化氢的乙酸溶液中加热醛来实现萘甲醛氧化为萘酚。使用该路线的产率始终低于理论值的40%。
将21.0 g 4-甲氧基-5,6,7,8-四氢萘酚溶于1 L圆底烧瓶中的100 mL丙酮中,用25 g精细研磨的无水碳酸钾(K2CO3)和26 g碘甲烷处理。混合物在蒸汽浴上回流2小时,冷却,并淬灭于1 L水中。试验萃取评估表明,起始苯酚以及产物醚均可从碱性水溶液中萃取到二氯甲烷中。水性反应混合物用3x60 mL二氯甲烷萃取,真空除去溶剂,残留物(19.6 g)在0.3 mm/Hg下于90-130 °C蒸馏,得到14.1 g起始原料和产物的油状白色固体混合物。将其在等重量的己烷下精细研磨,过滤除去残留的结晶固体。证明这些固体富含所需的醚。将其溶于己烷/二氯甲烷混合物(体积比3:1)中,并在硅胶制备柱上进行色谱分离,通过TLC连续监测洗脱液(使用该溶剂系统,产物醚的Rf为0.5,起始苯酚为0.1)。合并含有所需醚的馏分,真空除去溶剂,残留物重3.86 g,溶于1.0 mL己烷并用干冰冷却。低温过滤得到闪闪发光的白色晶体。分离出的5,8-二甲氧基四氢萘重量为2.40 g,熔点为44-45 °C。GCMS分析显示其主要为一种产物(m/s 192母峰和主峰),但未衍生的起始苯酚具有极差的GC性质,TLC仍然是化学纯度的最佳衡量标准。
将搅拌良好的3.69 g 5,8-二甲氧基四氢萘溶于35 mL二氯甲烷的溶液置于惰性气氛中,并用外部冰浴冷却至0 °C。然后慢速加入4.5 mL无水四氯化锡,产生短暂的颜色,迅速褪色为残留的黄色。然后加入2.0 mL二氯甲基甲基醚,导致立即变黑。搅拌几分钟后,让反应混合物恢复至室温,最后在蒸汽浴上温和回流。HCl的释放是连续的。然后将反应倒入200 mL水中,分层,水相用2x50 mL二氯甲烷萃取。合并有机相和萃取液,用3x50 mL 5%氢氧化钠洗涤,真空除去溶剂。残留物在0.3 mm/Hg下于120-140 °C蒸馏,得到3.19 g自发结晶的白色油状物。1,4-二甲氧基-5,6,7,8-四氢-2-萘甲醛的粗熔点为70-72 °C。来自己烷的分析样品熔点为74-75 °C。GCMS分析仅显示单一物质(m/s 220, 100%),没有明显的起始二甲氧基四氢萘存在。试图通过Vilsmeier程序(三氯氧磷和N-甲基甲酰苯胺)合成该醛,得到了复杂的产物混合物。使用丁基锂和二甲基甲酰胺(DMF)的合成努力仅得到回收的起始原料。
向1.5 g 1,4-二甲氧基-5,6,7,8-四氢-2-萘甲醛溶于20 g硝基甲烷的溶液中加入0.14 g无水乙酸铵,混合物在蒸汽浴上加热50分钟。反应速率通过TLC监测确定,在硅胶上以二氯甲烷为流动溶剂;醛的Rf为0.70,产物硝基苯乙烯的Rf为0.95。真空除去挥发物得到自发结晶的残留物。将获得的细小黄色晶体悬浮在1.0 mL甲醇中,过滤并风干,得到1.67 g 2,5-二甲氧基-β-硝基-3,4-(四亚甲基)苯乙烯,熔点为151.5-152.5 °C。分析元素(C14H17NO4):C,H。
给药剂量: 未知。
药效时长: 未知。
延伸和评论: 获得最终产品的道路让我想起了为什么在宇宙大爆炸后的最初几十亿年里,只有氢和氦。没有更重的元素。当一切膨胀到足以冷却到足以形成第一批实际物质时,所有的一切都只是充满活力的质子和中子。这些粒子相互碰撞,制造氘核,其中一些甚至一路碰撞成氦,但每当一个氦核与一个质量为一的粒子碰撞,试图形成质量为五的物质时,产物根本无法存在。锂-5和氦-5都具有不可能的半衰期,即10的负21次方秒。因此,在原始汤中,进入比氦更重的元素的唯一途径是相对稀少的重核之间发生碰撞,或者发生三体碰撞。从统计学上讲,这两种情况都是极其罕见的事件。如果有几个通过了,在质量8处还有另一个被禁止的障碍,因为铍-8的半衰期为10的负16次方秒。所以一切都必须等待几颗恒星燃烧殆尽,以便它们能够将足够的氦加工成重原子,以实现宇宙早期历史中不允许的一些核化学反应。
同样,在获得2C-G-4和G-4的过程中也遇到了两个几乎无法逾越的障碍。简单的甲基化芳香羟基的行为提供了只能通过一些非常复杂的手段才能分解成组分的混合物。当确实得到该产物时,将其转化为简单的芳香醛完全抗拒经典程序,要么给出复杂的混乱物,要么什么也没有。即使现在,随着这两个障碍的成功通过,推测简单的最后一步尚未完成。产物2C-G-4距离完成仅一步合成之遥(LAH还原),同样令人着迷的G-4也距离完成那最后一步还原。既然已经走过了最糟糕的沼泽,让我们进入实验室完成这一挑战。它们都将是活性化合物。